/mol)
(első elektron)
(Pauling szerint)
| Ne | 10 |
| 20,1797 | |
| 2s 2 2p 6 | |
| Neon | |
Neon- a nyolcadik csoport fő alcsoportjának eleme, D. I. Mengyelejev kémiai elemeinek periodikus rendszerének második periódusa, 10-es rendszámmal. Neon (Neon) szimbólummal jelölve. Az ötödik legnagyobb mennyiségben előforduló elem az Univerzumban (a hidrogén, a hélium, az oxigén és a szén után). Az egyszerű anyag, a neon (CAS-szám: 7440-01-9) inert, egyatomos gáz, szín, íz és szag nélkül.
A neont 1898 júniusában fedezte fel William Ramsay skót kémikus és Maurice Travers angol kémikus. Ezt az inert gázt a "kizárás módszerével" izolálták, miután az oxigént, a nitrogént és a levegő összes nehezebb komponensét cseppfolyósították. Az elem az egyszerű „neon” nevet kapta, amely görögül azt jelenti, hogy „új”. 1910 decemberében Georges Claude francia feltaláló egy neonnal töltött gázkisüléses lámpát készített.
név eredete
A név a görögből származik. νέος - új.
Van egy legenda, amely szerint az elem nevét Ramsay tizenhárom éves fia, Willie adta, aki megkérdezte apjától, hogy hívja majd az új gázt, megjegyezve, hogy szeretne nevet adni neki. novum(lat. – új). Apjának tetszett az ötlet, de úgy érezte, hogy a cím neon, amely egy görög szinonimából származik, jobban fog hangzani.
Terítés
A világ anyagában a neon egyenetlenül oszlik el, de általában az Univerzumban való elterjedtségét tekintve az ötödik helyen áll az összes elem között - körülbelül 0,13 tömegszázalék. A neon legmagasabb koncentrációja a Napban és más forró csillagokban, a gázködökben és a Naprendszer külső bolygóinak - Jupiter, Szaturnusz, Uránusz, Neptunusz - légkörében figyelhető meg. Számos csillag légkörében a neon a hidrogén és a hélium után a harmadik helyen áll.
földkéreg
A második periódus összes eleme közül neon- a Föld legkisebb népessége. A nyolcadik csoporton belül neon A földkéreg tartalmát tekintve a harmadik helyen áll – az argon és a hélium után. A gázködök és egyes csillagok sokszor több neont tartalmaznak, mint amennyi a Földön található.
A Földön a neon legmagasabb koncentrációja a légkörben figyelhető meg - 1,82 10 -3 térfogatszázalék, és teljes készletét 7,8 10 14 m³-re becsülik. 1 m³ levegő körülbelül 18,2 cm³ neont tartalmaz (összehasonlításképpen: ugyanannyi levegő csak 5,2 cm³ héliumot tartalmaz). A földkéreg átlagos neontartalma alacsony - 7·10-9 tömegszázalék. Összesen körülbelül 6,6 10 10 tonna neon található bolygónkon. A magmás kőzetek körülbelül 10 9 tonnát tartalmaznak ebből az elemből. Ahogy a kőzetek lebomlanak, gáz távozik a légkörbe. A légkört kisebb mértékben neon és természetes vizek látják el.
A tudósok bolygónk neonszegénységének okát abban látják, hogy a Föld egykor elvesztette elsődleges légkörét, amely magával vitte az inert gázok nagy részét, amelyek az oxigénhez és más gázokhoz hasonlóan nem tudtak kémiailag kötődni más elemekkel ásványi anyagokká és ezáltal megvesse a lábát a bolygón.
Meghatározás
A neont minőségileg emissziós spektrumokkal (585,25 nm és 540,05 nm karakterisztikus vonalak), kvantitatívan tömegspektrometriás és kromatográfiás elemzési módszerekkel határozzák meg.
Fizikai tulajdonságok
- A nemesgázok színtelen, egyatomos gázok, szín és szag nélkül.
- Az inert gázok nagyobb elektromos vezetőképességgel rendelkeznek, mint más gázok, és amikor áram halad át rajtuk, erősen világítanak, különösen a neon, tűzpiros fénnyel, mivel legfényesebb vonalai a spektrum vörös részén találhatók.
Neon emissziós spektrum (balról jobbra: ultraibolya-infravörös vonalak fehér színnel)
- Az inert gázok atommolekuláinak telítettsége abban is megmutatkozik, hogy az inert gázok cseppfolyósodási és fagyáspontja alacsonyabb, mint más azonos molekulatömegű gázoknak.
Kémiai tulajdonságok
Minden nemesgáz teljes elektronhéjjal rendelkezik, tehát kémiailag semleges. Kémiai tehetetlenség nem ő kivételes, ebben csak a hélium tud versenyezni vele. Eddig egyetlen vegyértékvegyületet sem sikerült előállítani. Még a neonnak vízzel (Ne 6H 2 O), hidrokinonnal és más anyagokkal alkotott úgynevezett klatrátvegyületeit is (a nehéz nemesgázok hasonló vegyületei – radon, xenon, kripton és még argon is széles körben ismerik) nagyon nehéz beszerezni és tartósítani. .
A Földön uralkodó könnyű nuklid, a 20 Ne forrását még nem sikerült megállapítani.
Úgy tartják, hogy a világűrben a neont is túlnyomórészt a 20 Ne fénynuklid képviseli. A meteoritokban sok 21 Ne és 22 Ne található, de ezek a nuklidok feltehetően magukban a meteoritokban keletkeznek kozmikus sugarak hatására az Univerzumban való utazásuk során.
A három stabil neonnuklidon kívül van még tizenhat instabil.
Nyugta
Neon a héliummal együtt a cseppfolyósítás és a levegő elválasztása során melléktermékként nyerik. Hélium elválasztás és nem ő adszorpció és kondenzáció miatt történik. Az adszorpciós módszer a képességen alapul nem ő a héliummal ellentétben adszorbeálódik (Ne + He tartalom akár 70%); a gázelegy extrakciós foka 0,5-0,6. Az nitrogéntől való végső tisztítás és a Ne és He elválasztása történhet szelektív adszorpcióval folyékony N2 hőmérsékletén, vagy kondenzációs módszerekkel - folyékony N2 ill. Korábban a neont inert közegként használták az iparban, de felváltotta az olcsóbb argon.
Elem szimbólum neoncsövekből
A neont gázkisüléses lámpák, rádióberendezésekben lévő jelzőlámpák, fotocellák és egyenirányítók töltésére használják.
Neon és hélium keverékét használják munkaközegként a gázlézerekben (hélium-neonlézer).
A neon és nitrogén keverékével töltött csövek vörös-narancssárga fényt adnak, amikor elektromos kisülés halad át rajtuk, ezért széles körben használják a reklámokban.
A neonlámpákat világítótornyokon és repülőtereken jelző célokra használják, mivel vörös színüket nagyon kevéssé szórja szét a köd és a pára.
Biológiai szerep
A neon nem játszik semmilyen biológiai szerepet.
Fiziológiai hatás
Az inert gázok élettani hatást fejtenek ki, ami a szervezetre gyakorolt kábító hatásukban nyilvánul meg. A neon (valamint a hélium) kábító hatását normál nyomáson a kísérletek nem rögzítik, míg megnövekedett nyomás esetén a „magas nyomású idegi szindróma” (HBP) tünetei korábban jelentkeznek.
Ebben a tekintetben a héliummal együtt a neon-hélium keverék részeként a neont is használják légzésre az óceánauták, búvárok és a magas nyomáson dolgozó emberek, hogy elkerüljék a gázembóliát és a nitrogén-narkózist. A keverék előnye, hogy kevésbé hűti a testet, mivel a neon hővezető képessége kisebb, mint a héliumé.
A könnyű neon-hélium levegő a légzési zavarokkal küzdő betegek állapotát is enyhíti.
A "neonfények" csak akkor felelnek meg a nevüknek, ha vörösen világítanak. Más színek előállításához bizonyos arányban higanyt és foszfort vagy más nemesgázt használnak.
Neon, Neon, Neon (10)
Kémiai elem neon Ramsay és Travers fedezte fel 1898-ban, néhány nappal a kripton felfedezése után. A tudósok mintát vettek a folyékony argon elpárolgása során keletkező első gázbuborékokból, és megállapították, hogy ennek a gáznak a spektruma egy új elem jelenlétét jelzi. Ramsay arról beszél, hogy nevet választott ennek az elemnek: „Amikor először megnéztük a spektrumát, ott volt a 12 éves fiam.”
Apa, mondta, mi ennek a neve gyönyörű gáz?
– Még nincs eldöntve – válaszoltam.
Ő új? - kérdezte kíváncsian a fiú.
Újonnan felfedezett- tiltakoztam.
Ilyenkor miért ne hívhatnánk Novum, apa?
Ez nem alkalmas, mert novum– Egy görög szó sem – válaszoltam.
Neonnak nevezzük, ami görögül újat jelent, innen kapta a nevét a gáz.
Az orosz nyelv nagyon gazdag és változatos. Gyakran tartalmaz olyan lexikai egységeket, amelyek más nyelvekből származnak. Gyakran előfordul, hogy egy szónak több jelentése van egyszerre. Az iskolázatlan emberek összezavarhatják őket, és bizonyos kifejezéseket helytelenül használhatnak. Hogy ez ne forduljon elő, érdemesebb a szó eredete, jelentése és alkalmazása iránt érdeklődni. Ma a neonról fogunk beszélni.
Mik a lehetőségek?
Kiderült, hogy ennek a szónak sok jelentése van. A neon egy kémiai elem és egyfajta hal. Ezt néha óriásplakátoknak is nevezik. A tinédzserek körében ezt a szót gyakran használják egy dal címeként vagy egy új láda neveként a játékban. Természetesen ez nem minden jelentés, amelyet ez a szó szerzett. De ezek a leggyakoribbak, ezért beszélünk róluk.
Kémia
Tehát kezdjük a leghíresebb, legnépszerűbb jelentéssel. A neon egy kémiai elem. A periódusos rendszer 18. csoportjában található. A rendszáma 10. Ne-ként jelöljük. Tulajdonságai szerint inert gáz, sem színe, sem szaga nincs.
Elbeszélés
Bár a neon valójában a semmiből jelent meg, William Ramsay és Maurice Travers tudósoknak köszönhetően bekerült a periódusos rendszerbe. Ezt egy kémiai vizsgálat után szerezték meg, amelyben az oxigén, a nitrogén és más komponensek cseppfolyósodtak. Így 1898-ban egy újabb kémiai elem vált ismertté a világ előtt.
Nevének görög gyökerei vannak. Amikor a neont felfedezték, az egyik vegyész fia azt javasolta, hogy apja nevezze az elemet „újnak” - latin módon. De Ramsay úgy döntött, hogy görög gyökereket ad ehhez a szóhoz. Úgy vélte, hogy a „neon” jobban hangzik, mint a „novum”.

Hol találom?
A neon meglehetősen gyakori elem. Az űrben és a földkéregben egyaránt megtalálható. Az első esetben nagyon egyenetlenül oszlik el. Azonban, mint korábban jeleztük, továbbra is az 5. helyen áll. A legtöbb neon a Napon és az összes többi „forró” csillagon található.
De a földkéregben ez a legkevésbé gyakori a többi elemhez képest. Bár a nyolcadik csoportjában a harmadik helyen áll az argon és a hélium után. Bolygónkon ez az elem a légkörben is jelen van, de rendkívül kis mennyiségben. A neon tömegének köszönhetően nem marad el a Földön, hanem közvetlenül a légkörbe kerül.
Használat
Ennek az elemnek a kis mennyisége ellenére használata még mindig meglehetősen gyakori. Kriogén berendezésekben van elhelyezve. Ott a hűtő szerepét tölti be. Korábban inert közegként is használták, de aztán kiderült, hogy az argon olcsóbb analóg. A gázkisüléses lámpákat leggyakrabban neonnal töltik meg. Ezért sokan ismerik ezt az elemet táblákról, fotocellákról és rádióberendezésekről.
Ha megtöltünk egy csövet neonnal és nitrogénnel, és áramot vezetünk át rajta, az narancsvörösre fog égni. Ez a technika gyakran látható a reklámokban. Természetesen előfordul, hogy a zöld fényt neonnak nevezhetjük. De ez nem teljesen igaz, mivel ebben az esetben leggyakrabban más gáz- vagy fluoreszcens bevonatot használnak.

vízi világ
Ha a szó másik jelentéséről beszélünk, érdemes megemlékezni a vízi világról. Ebben az esetben a neon a characin család hala. Kezdetben ezek a vízlakók az Amazonasban jelentek meg. Ezt a nevet a kémiai elem miatt adták, amelyről korábban beszéltünk. Először 1938-ban látták őket akváriumokban.
Ezek a halak nagyon népszerűek. A neonok fotói számos, az akváriumi halak tenyésztésével foglalkozó kiadványban láthatók. Ezek kicsi és fürge egyedek. Testük világító kékeszöld színű, farkuk élénkvörös. A hazai fajok akár 4 centiméteresre is megnőhetnek.
A neonok legközelebbi rokona a neon írisz. Ez a hal Új-Guinea folyójában él. Első pillantásra nagyon hasonlóak. De ha alaposan megnézzük, különböző formájúak, méretűek és színűek.
Egy kisállat
Kiderült, hogy a neonok tartalma nagyon egyszerű. Valószínűleg ezért találkozunk velük gyakran az akváriumokban. Ezek a halak szerények. Még egy kezdő is könnyen kezelheti őket ebben a kérdésben. Egyes források szerint a neonok 18-28 fokos vízben is élhetnek. De a gyakorlatban a helyzet némileg más. A neonok számára még mindig kényelmesebb lesz 20-22 fokos hőmérsékleten élni. Ekkor akár 4 évig is maradhatnak ilyen környezetben.

Annak érdekében, hogy a neonok hosszabb ideig örömet szerezzenek, jobb, ha megvédjük őket a szállítással vagy átszállítással járó stressztől. Jobb is, ha olyan helyre helyezzük őket, ahol több a megfelelőjük. Kényelmesebb nekik falkában élni (legalább 5-6 darab). A levegőztetéshez jobb, ha permetezőt használunk, hogy elkerüljük a folyamatos áramlást. Jól. Végül a neon csecsemőket bármilyen étellel kell etetni, kivéve az élő vagy fagyasztott vérférgeket.
Játékértelmezés
Sok tinédzser ismeri a Warface játékot. A neon számukra nem kémiai elem vagy hal, hanem fegyvertok. Tavaly év végén jelent meg a játékban. Most megvásárolhatja a projekt webhelyén vagy a játékon belüli boltban 4 ezer rubelért.
Azok számára, akik keveset értenek a számítógépes játékokhoz, íme néhány rövid információ. "Warface" - A játék ingyenes és online. A projekt jól ismert analógja a „KS”. Annak ellenére, hogy a játék ingyenes, még mindig lehet rá adományozni, különben hogyan gyűjtene pénzt a projekt fejlesztésre?
A Warface speciális, továbbfejlesztett fegyvereket tartalmaz, amelyek lehetővé teszik a játékosok számára, hogy uralják a többi játékost. Az egyik ilyen doboz neve „Neon”. Tartalmaz egy gépkarabélyt, egy sörétes puskát, egy géppisztolyt és egy mesterlövész puskát. Mindegyik javított pusztító erővel, van, amelyik csökkentette a visszarúgást, néhány lövési pontosságot és megnövelt tempót kapott.

A Neon tok egyfajta erősítő, amely segít a tulajdonosnak erősebbé válni ellenfelénél. A játékfejlesztők különleges eredményekkel is előálltak azok számára, akik megvásárolták ezt az arzenált.
Zene
Mint korábban említettük, a „neon” szó meglehetősen kétértelmű. Nemcsak a kémiában, a biológiában vagy a számítógépes játékokban, hanem a zenében is megtalálható. Sokan ismerik a fáraó „Neon” című dalát. Nemrég jelent meg. Manapság nagyon népszerű a rapper rajongói körében.
A szerző maga az előadó, Gleb Gennadievich Golubin. Most 20 éves, nemcsak orosz hip-hop és cloud rapper, hanem két nagy kreatív egyesület vezetője is. A Pharaoh egyébként LSP zenésszel együtt rögzítette a „Neon” című számot. A rap közösségben is nagyon népszerű szerző és előadó. Eredetileg Fehéroroszországból származik.

A dalról
A „Neon” dal szövege egészen egyedi. Még mindig a két rapper stílusában. A premierre 2016. szeptember végén került sor. A szám egy lányról szól, és arról, hogy egy srác hogyan akar vele táncolni. A főszereplő maga bocsát ki neonfényt: „Az én neonomban, táncolj az én neonomban...” Egyébként a szám jelentéséről nem is kell beszélni, hiszen inkább klubbulira tervezték.
Egyéb opciók
A fenti eseteken kívül a „neon” szó megtalálható a különböző létesítmények nevében. Ezek közé tartoznak a FÁK-szerte működő klubok, valamint tánc- és fitneszstúdiók. És építőipari cégek is. De leggyakrabban ilyen nevű reklámcégeket találhat, amelyek világítástervezéssel, táblák gyártásával, kültéri reklámozással stb.
Egyébként van még pár olyan mű is, amit „Neonnak” hívnak. Vannak köztük szakkönyvek technológusoknak és szépirodalom is. Az utóbbiban a neon metafora vagy szójáték.
A neon kémiai elem széles körben elterjedt az Univerzumban, de a Földön meglehetősen ritka. Megtanulták azonban, hogy a világűr látogatása nélkül szerezzék be, és most az iparban, rádió- és fényképészeti berendezések gyártására, valamint mélytengeri búvárkodásra használják. Mi az a neon? Milyen tulajdonságokkal és tulajdonságokkal rendelkezik? Erről fogunk beszélni.
Mi az a neon?
Mengyelejev periódusos rendszerében ez az elem a nyolcadik csoportban, a tizedik helyen található. Ezt a Ne szimbólum jelöli. Egyszerű anyagként monoatomos gáz, amely szagtalan, színtelen és íztelen.
Három izotóp formájában létezik: 20 Ne, 21 Ne és 22 Ne, amelyek a természetben stabilak. A leggyakoribb nuklid a 20 Ne. Bolygónk légkörében előfordulása közel 90%, míg a 22 Ne izotópnál 9,25%, a 21 Ne izotópnál pedig csak 0,27%. Az utolsó két izotóp elsősorban a kozmikus sugárzás hatására jön létre, amely a nátrium, a szilícium, az alumínium és más elemek magjait érinti. Ezért a Földön leggyakrabban a levegőben vannak jelen, és nem a vízben vagy a földkéregben. A Neon-20 kialakulásának forrása bolygónkon még mindig ismeretlen. Ezeken az izotópokon kívül körülbelül 16 instabil nuklidot izoláltak, amelyek bomlási ideje 9 zeptoszekundum és 3,38 perc közötti.
A felfedezés története
Hogy mi a neon, az csak a 19. század végén vált ismertté. Ezt megelőzően a tudomány csak két inert gázt fedezett fel - az argont és a héliumot, amelyek a periódusos rendszer első és harmadik periódusát foglalják el. Ugyanakkor a második periódus helye üresen maradt, így a kutatók még legalább egy hasonló anyag létezését feltételezték a természetben. 1997-ben a skót kémikus, Ramsay még egy jelentést is szentelt neki, amelyet „Felfedezetlen gáz” címmel. A következő évben pedig volt szerencséje felfedezni a hiányzó elemet.
Ennek megtalálásához a tudós héliumot és aragont elemzett, tanulmányozta az ásványok összetételét, de a siker akkor jött, amikor a levegő felé fordult. A gázelegyet cseppfolyósította és lassan elpárologtatta, majd egy speciális elektromos árammal működő kisülőcsövön keresztül frakciókra juttatta. A fel nem fedezett anyagnak a héliumhoz közeli tulajdonságokkal kellett volna rendelkeznie, ezért Ramsay abban reménykedett, hogy a legkönnyebb frakcióban találja meg, amely előbb elpárolog.
És így történt. A csőben lévő elektronokkal kölcsönhatásba lépve a levegő első része izzani kezdett, és a hélium és argon spektruma mellett a tudós más vonalakat is látott. Megerősítették egy korábban ismeretlen gáz létezését. Ramsay a görög „neon” nevet adta a felfedezett elemnek, ami „új”-ot jelent.
Tulajdonságok
Hogy mi a neon, azt a fizikai és kémiai tulajdonságai alapján lehet leginkább megítélni. Ez a gáz az egyik legkönnyebb. Sűrűsége 0,0089999 g/cm³. Forráspontja –246,05 °C, olvadáspontja –248,6 °C.
A neon gyakorlatilag nem lép reakcióba más anyagokkal. Nehéz feladni vagy megszerezni az elektronokat, ezért a nemesgázok közé sorolják. Tehetetlenség szempontjából csak a hélium hasonlítható hozzá. Eddig egyetlen vegyértékvegyületet sem sikerült előállítani. Vízben gyengén oldódik, de az aktív szén jól adszorbeálja.
Más nemesgázokhoz hasonlóan jó elektromos vezetőképességgel rendelkezik. Ha nagyfeszültségű áramot vezet át rajta, akkor világítani kezd. A gáz spektrumában körülbelül 900 különböző színű vonal található, de ezek közül a legfényesebb a vörös és a narancssárga. A neonnak ezt a tulajdonságát széles körben alkalmazták a kültéri reklámozás területén. Tizenkét évvel a megnyitó után pirosan világító táblák kezdtek megjelenni az utcákon, boltok és kávézók nevével. Az első szabadalmat a Claude Neon Lights Inc. bocsátotta ki rájuk.

Elterjedés a természetben
A neont vagy a Ne-t nevezhetjük földönkívüli gáznak, mert a világűrben és más csillagászati objektumokban sokkal több van belőle, mint bolygónkon. Különösen sok van belőle az Uránusz, Neptunusz, Szaturnusz, Jupiter légkörében, ködökben és nagyon forró csillagokban. Ezenkívül meteoritokban és más kozmikus testekben is megtalálható.

Az egész Univerzumban a gáz az ötödik helyen áll a hidrogén, a hélium, az oxigén és a szén mögött. Tartalma körülbelül 0,13 tömeg%.
A Földön ritka elemnek számít. A földkéreg körülbelül 7,10–9%-ban, az óceánvizekben és a sós tározókban körülbelül 2,10–8%-ban található meg. Ennek a kémiai elemnek a legmagasabb koncentrációja a bolygó légkörében figyelhető meg, ahol 1,82·10-3 térfogatszázalék a tartalma.
Hogyan kapod meg?
A neon kőzetekben és vízben való alacsony előfordulása miatt fő forrása a légköri levegő. Erős hűtéssel nyerik ki belőle a gázt. A folyékony nitrogén hőmérsékletén a neon kristályosodik, és könnyen elválik a héliumtól, amely gáz halmazállapotú marad.

A levegőből nitrogén és oxigén kivonása során melléktermékként is nyerhető. Ebben az esetben aktív szén adszorpciót alkalmaznak a gáz leválasztására. A neon meghatározásához általában spektrális sugárzást vagy kromatográfiás analízist alkalmaznak.
Felhasználási területek
A neon kémiai elemet ma is használják feliratokban és reklámszalagokon, és más anyagokkal keverve is különböző színeket állítanak elő. A héliummal együtt lézerek gyártásához, és függetlenül - fényképészeti berendezések gyártásához használják.

A folyékony neon hőkapacitása jobb, mint a hélium, és sokkal olcsóbb is. A hidrogénnel együtt hűtőközegként használják különféle hűtőegységekben. Ezeken a gázokon alapuló kriogén kamrákra van szükség az orvostudományban az élő szövetek lefagyasztásához. A neon és hélium keverékét a légzési nehézségekkel küzdő betegek állapotának enyhítésére használják, erre a célra nitrogénmentes levegővel feltöltött helyiségekben osztják el.
A vegyi anyagok periódusos rendszerének összes eleme között érdekes tulajdonságokkal rendelkezik az olyan csoport, mint az inert gázok. Ide tartozik az argon, a neon, a hélium és néhány más anyag. Mi a neon, és hol használják ezt a gázt széles körben a modern világban?
A neon felfedezésének története
A periódusos rendszer nem volt azonnal feltöltve minden kémiai elemmel, így egyes csoportokban és periódusokban hiányosságok mutatkoztak. Így a vegyészek új anyagok felfedezését jósolták, ami a neonnál történt. Ramsay Rayleigh vegyész volt az első tudós, aki elgondolkodott a neon létezésén. Ekkor fedezték fel a két legközelebbi inert gázt: az argont és a héliumot, de a táblázat köztes cellája üres volt. A tudós azt feltételezte, hogy az új elem atomtömege 20, a hidrogénsűrűsége pedig 10, azt azonban nem tudni, hogy mi a neon a természetben.
Hogyan tudta Ramsay elkülöníteni a neont és bebizonyítani a létezését? Kísérletében egy szokásosat használt, amelyet először cseppfolyósított, majd lassan elpárologtatott. Az így kapott gáznemű frakciókat kisülési csőben tanulmányozták, amely lehetővé tette az anyagok spektrumvonalainak megtekintését. Ezen a vonalon találtak egy új elemet.
Az univerzumban a hatodik leggyakoribb elem a neon. A szó jelentése görögül „új”. Kezdetben Ramsay fia, Willie azt javasolta, hogy az új elemet novumnak nevezzék, ami egyben „új”-t is jelent, de apja úgy döntött, hogy a szót kissé neonra változtatja, ami szerinte jobban hangzik.
A neon tulajdonságai
Ez az inert gáz az argon és a hélium közötti periódusos rendszerben található, ami ezen anyagok köztes tulajdonságait adja. A neonnak két energiaszintje van, 2 és 8 elektronnal. Ez a tulajdonság közvetlenül befolyásolja a gáz reakcióképességét, mert más elemekkel nem képez vegyületeket.

Mi a neon kémiai szempontból? Ez egy könnyű gáz, amely -245,98 °C hőmérsékleten cseppfolyósodik, forráspontja 2,6 °C. A gáz vízoldhatósága nagyon alacsony, de a neon aktív szénen való adszorpciója lehetővé teszi a tiszta gáz elválasztását a szennyeződésektől.
Mi a neon fizika szempontból? Ez egy gáz, amely az áram hatására élénkvörös és narancssárga spektrumokra oszlik. amelyet egyidejűleg bocsát ki, nagyon stabil és fényes. Ennek a jelenségnek a fizikája magában foglalja azt, hogy az elektronok neonatomokba ütköznek, és fényfotonokat bocsátanak ki.
Hol van a neon
Az univerzumban a neon a 6. legelterjedtebb elem a hélium, a hidrogén és számos más elem után. Ez az inert gáz viszonylag nagy mennyiségű csillagot és vörös bolygót foglal el. A Plútó tanulmányozása során felmerült, hogy légköre teljes egészében neonból áll, és az alsóbb rétegekben ez a gáz cseppfolyósodik a bolygó kritikusan alacsony hőmérséklete miatt.

Ami a Földet illeti, a neon a legtöbbet a légkörben (0,00182%), a földkéregben pedig nagyon kevés. Úgy gondolják, hogy a nemesgázok képtelenek kötődni más elemekkel és ásványi anyagokat képezni, ez volt a fő oka annak, hogy ezek az anyagok kis mennyiségben maradtak a Földön.
neon használata
Napjainkra a gyártásban a neon iránti kereslet jelentősen megnőtt, ami folyamatos hiányt jelent. Ennek oka az a tény, hogy a tiszta inert gáz felszabadulása meglehetősen hosszú ideig tart, és a levegő tartalma nagyon alacsony.
A neont az iparban hűtőfolyadékként használják a kriogén technológiában. A rakéta-üzemanyagot folyékony neon hőmérsékleten tárolják, az állati és növényi szöveteket, a vegyi anyagokat pedig lefagyasztják. A neonkristályokban optimális feltételek jönnek létre a nagyon összetett, hőt nem tűrő reakciók lezajlásához (H2O2, oxigén-fluoridok szintézise stb.).
Egyes lámpák és lámpatestek neont is használnak. Ennek a gáznak, mint fényforrásnak nagyon nagy a jelentősége, mert fénye nagy távolságra is látható. világítótornyokra, repülőtéri sávokra, sokemeletes tornyokra történő telepítéshez használják. Egyes szöveges hirdetéseket neon alapú lámpákkal világítanak meg.

Az ilyen lámpákban a neon nem tiszta formában. Mindig megfelelő arányban keverik argonnal, ami narancssárga színt ad a fénynek. Ez azonban semmilyen módon nem rontja a jó láthatóság tulajdonságait, mert Az ilyen lámpák bármilyen kedvezőtlen időjárási körülmény között és nagy távolságokon láthatók.
MEGHATÁROZÁS
Neon- az inert (nemes) gázok osztályába tartozó kémiai elem. Az alcsoport VIII. A csoportjának második periódusában található, ha a rövid periódusos táblázatot nézzük, vagy a 18. csoportban, ha a hosszú periódusos táblázatot nézzük.
A sorozatszám 10. A nukleáris töltés +10. Atomtömeg - 20,179 amu.
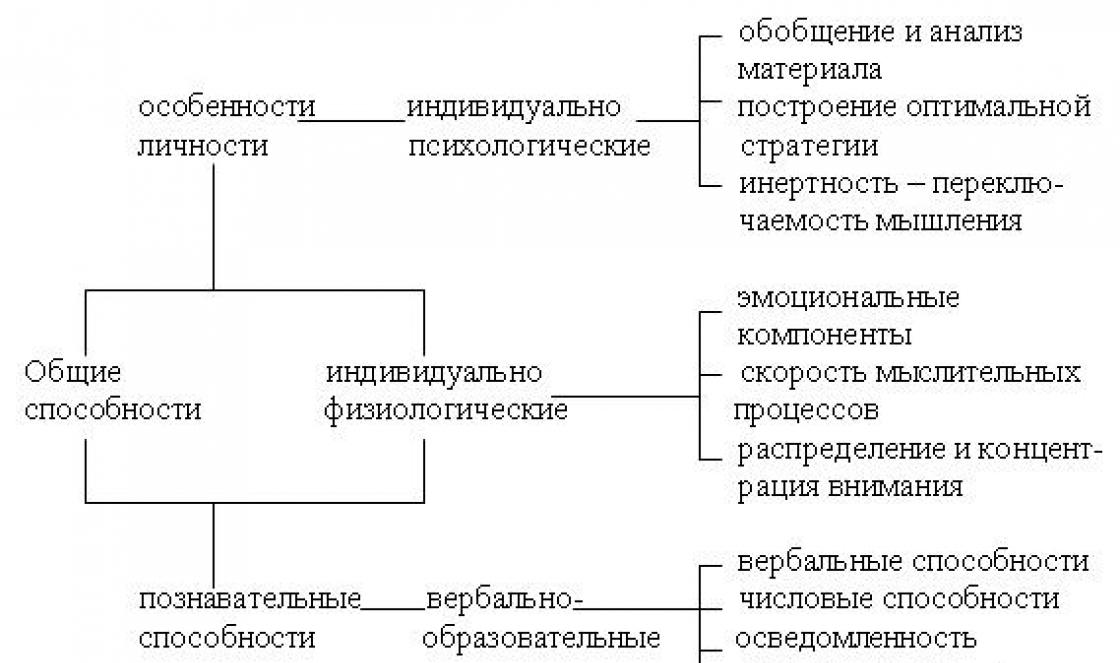
A neonatom elektronikus szerkezete
A neonatom egy pozitív töltésű magból (+10) áll, amely körül 10 elektron mozog atomburokban (pályákon). Mivel a neon a második periódusban található, ebből a kagylóból kettő van. A hélium atom szerkezetét az 1. ábra mutatja:
Rizs. 1. A neonatom szerkezete.
A neonatom elektronikus konfigurációja kétféleképpen írható fel:
1s 2 2s 2 2p 6 .
A neon a p-elemek családjába tartozik. A neonatom energiadiagramja így néz ki:

A neonatom energiaszintje teljes, mivel a p-pálya mindössze hat elektront tud befogadni. Ezért a neont inert gáznak minősítik. Kémiailag inaktív.
Példák problémamegoldásra
1. PÉLDA