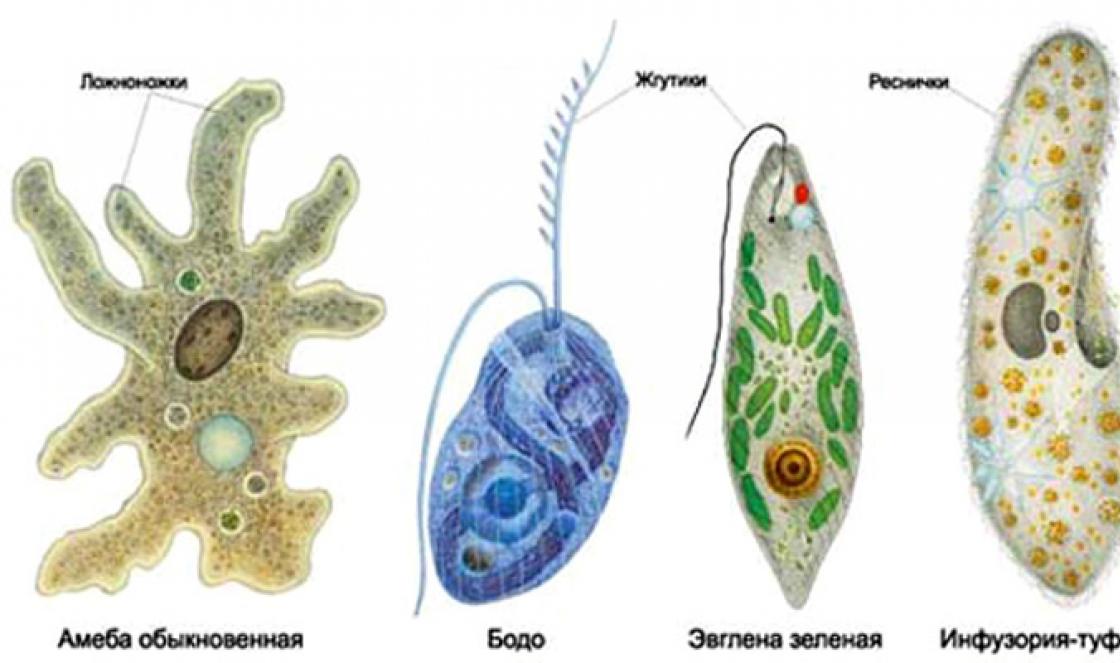
Mikroorganismy (mikroby) jsou jednobuněčné organismy o velikosti menší než 0,1 mm, které nejsou pouhým okem vidět. Patří sem bakterie, mikrořasy, některé nižší vláknité houby, kvasinky a prvoci (obr. 1). Mikrobiologie je studuje.
Rýže. 1. Mikrobiologické objekty.
Na Obr. 2. Můžete vidět některé zástupce jednobuněčných prvoků. Někdy objekty této vědy zahrnují nejprimitivnější organismy na Zemi - viry, které nemají buněčnou strukturu a jsou komplexy nukleových kyselin (genetického materiálu) a bílkovin. Častěji jsou izolovány do zcela samostatného studijního oboru (virologie), protože mikrobiologie je spíše zaměřena na studium mikroskopických jednobuněčných organismů.

Rýže. 2. Jednotliví zástupci jednobuněčných eukaryot (protozoa).
Nauky algologie a mykologie, které studují řasy, respektive houby, jsou samostatnými disciplínami, které se při studiu mikroskopických živých objektů překrývají s mikrobiologií. Bakteriologie je skutečným odvětvím mikrobiologie. Tato věda se zabývá výhradně studiem prokaryotických mikroorganismů (obr. 3).

Rýže. 3. Schéma prokaryotické buňky.
Na rozdíl od eukaryot, mezi které patří všechny mnohobuněčné organismy, stejně jako prvoci, mikroskopické řasy a houby, nemají prokaryota vytvořené jádro obsahující genetický materiál a skutečné organely (trvalé specializované struktury buňky).
Mezi prokaryota patří pravé bakterie a archaea, které jsou podle moderní klasifikace označovány jako domény (superříše) Archaea a Eubacteria (obr. 4).

Rýže. 4. Oblasti moderní biologické klasifikace.
Strukturní vlastnosti bakterií
Bakterie jsou důležitým článkem koloběhu látek v přírodě, rozkládají rostlinné a živočišné zbytky, čistí vody kontaminované organickou hmotou a upravují anorganické sloučeniny. Bez nich by život na Zemi nemohl existovat. Tyto mikroorganismy jsou distribuovány všude, v půdě, vodě, vzduchu, živočišných a rostlinných organismech.
Bakterie se liší v následujících morfologických rysech:
- Tvar buňky (kulatý, tyčovitý, vláknitý, stočený, spirálový, stejně jako různé přechodové možnosti a konfigurace ve tvaru hvězdy).
- Přítomnost zařízení pro pohyb (nehybné, bičované, kvůli sekreci hlenu).
- Vzájemné skloubení buněk (izolované, spojené ve formě párů, granulí, větvících se forem).
Mezi strukturami tvořenými kulatými bakteriemi (koky) jsou buňky, které jsou po rozdělení v párech a poté se rozpadnou na jednotlivé útvary (mikrokoky) nebo zůstávají stále pohromadě (diplokoky). Kvadratickou strukturu čtyř buněk tvoří tetrakoky, řetězec streptokoky, granule 8-64 jednotek sarcina a shluky stafylokoky.
Tyčinkovité bakterie jsou reprezentovány různými tvary díky velké variabilitě délky (0,1-15 µm) a tloušťky (0,1-2 µm) buňky. Tvar posledně jmenovaného závisí také na schopnosti bakterií tvořit spory - struktury s tlustým obalem, který umožňuje mikroorganismům přežít nepříznivé podmínky. Buňky s touto schopností se nazývají bacily a ty, které takové vlastnosti nemají, se jednoduše nazývají tyčinkovité bakterie.
Speciálními modifikacemi tyčinkovitých bakterií jsou vláknité (protáhlé) formy, řetězce a větvené struktury. Ten je v určité fázi vývoje tvořen aktinomycetami. „Zakřivené“ tyčinky se nazývají zvlněné bakterie, mezi nimiž jsou izolována vibria; spirilla se dvěma ohyby (15-20 um); spirochety, které připomínají vlnovky. Jejich délky buněk jsou 1-3, 15-20 a 20-30 um. Na Obr. Obrázky 5 a 6 ukazují hlavní morfologické formy bakterií a také typy uspořádání spor v buňce.

Rýže. 5. Základní formy bakterií.

Rýže. 6. Bakterie podle typu umístění spor v buňce. 1, 4 – uprostřed; 2, 3, 5 – koncové umístění; 6 – ze strany.
Hlavní buněčné struktury bakterií: nukleoid (genetický materiál), ribozomy určené k syntéze bílkovin, cytoplazmatická membrána (součást buněčné membrány), která je u mnoha zástupců navíc chráněna shora, pouzdro a slizniční obal (obr. 7).

Rýže. 7. Schéma bakteriální buňky.
Podle klasifikace bakterií existuje více než 20 typů. Například extrémně termofilní (milovníci vysokých teplot) Aquificae, anaerobní tyčinkovité bakterie Bacteroidetes. Nejdominantnějším kmenem, který zahrnuje různé zástupce, je však Actinobacteria. Zahrnuje bifidobakterie, laktobacily a aktinomycety. Jedinečnost posledně jmenovaného spočívá ve schopnosti tvořit mycelium v určité fázi vývoje.
V běžné řeči se tomu říká mycelium. Větvící se buňky aktinomycet skutečně připomínají houbové hyfy. Navzdory této vlastnosti jsou aktinomycety klasifikovány jako bakterie, protože jsou prokaryota. Jejich buňky jsou přirozeně strukturou méně podobné houbám.
Aktinomycety (obr. 8) jsou pomalu rostoucí bakterie, a proto nemají schopnost soutěžit o snadno dostupné substráty. Jsou schopny rozkládat látky, které jiné mikroorganismy nemohou využít jako zdroj uhlíku, zejména ropné uhlovodíky. Aktinomycety jsou proto intenzivně studovány v oblasti biotechnologií.
Někteří zástupci se koncentrují v oblastech ropných polí a vytvářejí speciální bakteriální filtr, který zabraňuje pronikání uhlovodíků do atmosféry. Aktinomycety jsou aktivními producenty prakticky cenných sloučenin: vitamínů, mastných kyselin, antibiotik.

Rýže. 8. Reprezentativní aktinomyceta Nocardia.
Houby v mikrobiologii
Předmětem mikrobiologie jsou pouze houby nižších plísní (zejména rhizopus, mucor). Jako všechny houby nejsou schopny samy syntetizovat látky a vyžadují živné médium. Mycelium nižších představitelů tohoto království je primitivní, nerozdělené přepážkami. Zvláštní niku v mikrobiologickém výzkumu zaujímají kvasinky (obr. 9), vyznačující se absencí mycelia.

Rýže. 9. Formy kolonií kvasinkových kultur na živném médiu.
V současné době bylo shromážděno mnoho poznatků o jejich prospěšných vlastnostech. Kvasinky jsou však nadále studovány pro svou schopnost syntetizovat prakticky cenné organické sloučeniny a jsou aktivně využívány jako modelové organismy v genetických experimentech. Od starověku se kvasnice používaly při fermentačních procesech. Metabolismus se u různých zástupců liší. Proto jsou některé kvasinky pro určitý proces vhodnější než jiné.
Například Saccharomyces beticus, který je odolnější vůči vysokým koncentracím alkoholu, se používá k vytvoření silných vín (až 24 %). Zatímco kvasinky S. cerevisiae jsou schopny produkovat nižší koncentrace ethanolu. Podle oblastí použití se kvasinky dělí na krmiva, pekaře, pivovary, lihoviny a vína.
Patogenní mikroorganismy
Všude se vyskytují choroboplodné nebo patogenní mikroorganismy. Spolu se známými viry: chřipka, hepatitida, spalničky, HIV atd. jsou nebezpečnými mikroorganismy rickettsie a také streptokoky a stafylokoky, které způsobují otravu krve. Mezi tyčinkovitými bakteriemi je mnoho patogenů. Například záškrt, tuberkulóza, břišní tyfus (obr. 10). Mezi prvoky se vyskytuje řada zástupců pro člověka nebezpečných mikroorganismů, zejména malarické plasmodium, toxoplasma, leishmania, lamblia, trichomonas a patogenní améby.

Rýže. 10. Fotografie bakterie Bacillus anthracis, která způsobuje antrax.
Mnohé aktinomycety nejsou nebezpečné pro lidi a zvířata. Mezi mykobakteriemi, které způsobují tuberkulózu a lepru, se však nachází mnoho patogenních zástupců. Některé aktinomycety iniciují onemocnění, jako je aktinomykóza, doprovázené tvorbou granulomů a někdy i zvýšením tělesné teploty. Některé druhy plísní jsou schopny produkovat látky toxické pro člověka – mykotoxiny. Například někteří zástupci rodu Aspergillus, Fusarium. Patogenní houby způsobují skupinu onemocnění zvanou mykózy. Kandidózu nebo jednoduše řečeno soor způsobují kvasinky podobné houbám (obr. 11). V lidském těle jsou vždy přítomny, ale aktivují se pouze při oslabení imunitního systému.

Rýže. 11. Původcem drozdů je houba Candida.
Plísně mohou způsobit různé kožní léze, zejména všechny druhy lišejníků, kromě herpes zoster, který je způsoben virem. Kvasinky Malassezia, stálí obyvatelé lidské kůže, mohou způsobit snížení aktivity imunitního systému. Nespěchejte si hned umýt ruce. Kvasinky a oportunní bakterie v dobrém zdravotním stavu plní důležitou funkci, brání rozvoji patogenních mikroorganismů.
Viry jako předmět mikrobiologie
Viry jsou nejprimitivnější organismy na Zemi. Ve volném stavu v nich neprobíhají žádné metabolické procesy. Teprve když vstoupí do hostitelské buňky, začnou se viry množit. Ve všech živých organismech je nositelem genetického materiálu kyselina deoxyribonukleová (DNA). Pouze mezi viry jsou zástupci s genetickou sekvencí jako je ribonukleová kyselina (RNA).
Viry často nejsou klasifikovány jako skutečně živé organismy.
Morfologie virů je velmi různorodá (obr. 12). Typicky se jejich průměrná velikost pohybuje od 20 do 300 nm.

Rýže. 12. Diverzita virových částic.
Někteří zástupci dosahují délky 1-1,5 mikronu. Struktura viru spočívá v obklopení genetického materiálu speciálním proteinovým rámcem (kapsidou), který se vyznačuje různými tvary (helikální, ikosaedrický, sférický). Některé viry mají navrchu obal vytvořený z membrány hostitelské buňky (superkapsida). Například (obr. 13) je známý jako původce onemocnění zvaného (AIDS). Obsahuje RNA jako genetický materiál a ovlivňuje určitý typ buněk imunitního systému (pomocné T-lymfocyty).

Rýže. 13. Struktura viru lidské imunodeficience.
Výživa bakterií.
Výživa.
Pasivní difúze
Usnadněná difúze
Aktivní transport
V prvním případě tvoří molekula živiny komplex s proteinem periplazmatického prostoru, který interaguje se specifickou permeázou cytoplazmatické membrány. Po energeticky závislém průniku cytoplazmatickou membránou se komplex „substrát – periplazmatický protein – permeáza“ disociuje s uvolněním molekuly substrátu.
Během aktivního transportu s chemickou modifikací transportované látky řetězec dějů zahrnuje: (1) fosforylaci membránového enzymu-2 z cytoplazmy fosfoenolpyruvátem; (2) vazba molekul substrátu fosforylovaným enzymem-2 na povrch cytoplazmatické membrány; (3) energeticky závislý transport molekuly substrátu do cytoplazmy; (4) přenos fosfátové skupiny na molekulu substrátu; (5) disociace komplexu „substrát-enzym“ v cytoplazmě. Vlivem fosforylace se molekuly substrátu hromadí v cytoplazmě buněk a nejsou schopny je opustit.
Klasifikace bakterií podle druhu výživy.
Podle způsobu příjmu živin látky bakterie se dělí na holofyty A Holozoans. Holofytické bakterie (z řečtiny holos- kompletní a fyticos– související s rostlinami) nejsou schopny uvolňovat do prostředí enzymy, které rozkládají substráty, v důsledku čehož spotřebovávají živiny výhradně v rozpuštěné, molekulární formě. Holozoální bakterie (z řečtiny holos- kompletní a zoikos- související se zvířaty), naopak mají komplex exoenzymů, které zajišťují vnější výživu - rozklad substrátů na molekuly mimo bakteriální buňku. Poté molekuly živin vstupují do holozoálních bakterií.
Podle zdroje uhlíku mezi bakteriemi jsou izolovány autotrofy A heterotrofy. Autotrofy (z řečtiny auta- moje maličkost, trofej– potraviny) jako zdroj uhlíku se používá oxid uhličitý (CO 2), ze kterého se syntetizují všechny látky obsahující uhlík. Pro heterotrofy (z řeckého geteros - další a trofej– potraviny) zdrojem uhlíku jsou různé organické látky v molekulární formě (sacharidy, vícesytné alkoholy, aminokyseliny, mastné kyseliny). Největší stupeň heterotrofie je vlastní prokaryotům, která mohou žít pouze uvnitř jiných živých buněk (například rickettsie a chlamydie).
Zdrojem dusíku Prokaryota se dělí do 3 skupin: 1) bakterie fixující dusík (asimilují molekulární dusík z atmosférického vzduchu); 2) bakterie, které spotřebovávají anorganický dusík z amonných solí, dusitanů nebo dusičnanů; 3) bakterie, které asimilují dusík obsažený v organických sloučeninách (aminokyseliny, puriny, pyrimidiny atd.).
Podle zdroje energie bakterie se dělí na fototrofy A chemotrofy. Fototrofní bakterie , stejně jako rostliny, jsou schopny využívat sluneční energii. Fototrofní prokaryota nezpůsobují onemocnění u lidí. Chemotrofní bakterie získat energii z redoxních reakcí.
Podle povahy donorů elektronů litotrofy(z řečtiny litos- kámen) a organotrofy. U litotrofy (chemolithotrofy ) anorganické látky (H 2, H 2 S, NH 3, síra, CO, Fe 2+ atd.) působí jako donory elektronů. Dárci elektronů organotrofy (chemoorganotrofy ) jsou organické sloučeniny - sacharidy, aminokyseliny atd.
Většina bakterií patogenních pro člověka má chemoorganotrofní (chemoheterotrofní) typ výživy; Chemolithotrofní (chemoautotrofní) typ je méně častý.
Podle schopnosti syntetizovat organické sloučeniny chemotrofní bakterie se dělí na prototrofy, auxotrofy A hypotrofy. Prototrofní bakterie syntetizovat všechny potřebné organické látky z glukózy a amonných solí. Bakterie jsou tzv auxotrofy , pokud nejsou schopny syntetizovat jakoukoli organickou hmotu ze specifikovaných sloučenin. Extrémní stupeň ztráty metabolické aktivity se nazývá malnutrice. Hypotrofní bakterie zajišťují jejich životní funkce reorganizací struktur nebo metabolitů hostitele.
Kromě uhlíku a dusíku potřebují bakterie k plnému životu síru, fosfor a kovové ionty. Zdrojem síry jsou aminokyseliny (cystein, methionin), vitamíny, kofaktory (biotin, kyselina lipoová aj.), sírany. Zdrojem fosforu jsou nukleové kyseliny, fosfolipidy a fosfáty. V dostatečně vysokých koncentracích potřebují bakterie hořčík, draslík, vápník a železo; v mnohem menších - zinek, mangan, sodík, molybden, měď, nikl, kobalt.
Růstové faktory- to jsou látky, které si bakterie nedokážou samy syntetizovat, ale nutně je potřebují. Růstové faktory mohou zahrnovat aminokyseliny, dusíkaté báze, vitamíny, mastné kyseliny, porfyriny železa a další sloučeniny. Pro vytvoření optimálních podmínek pro život bakterií je nutné do živných médií přidávat růstové faktory.
Metabolismus, přeměna energie
A) Konstruktivní metabolismus.
Povinnou fází bakteriální výživy je asimilace živin, to znamená jejich zařazení ve změněné nebo modifikované formě do syntetických reakcí za účelem reprodukce buněčných složek a struktur.
Metabolismus bílkovin u bakterií se může vyskytovat ve 3 fázích: primární štěpení bílkovin, sekundární štěpení a syntéza bílkovin. Primární rozklad proteinových molekul na peptony provádějí exoenzymy - exoproteázy vylučované bakteriemi do prostředí. Sekundární rozklad nastává působením endoenzymů (endoproteáz), které mají všechny bakterie. Tento proces probíhá uvnitř bakteriální buňky a spočívá v rozkladu peptidů na jejich základní aminokyseliny. Posledně jmenované mohou být použity nezměněné nebo podrobeny chemickým přeměnám (deaminace, dekarboxylace atd.), v důsledku čehož se objeví amoniak, indol, sirovodík, ketokyseliny, alkohol, oxid uhličitý atd diagnostická hodnota v bakteriologii.
Spolu s reakcemi rozpadu bílkovin dochází k reakcím jejich syntézy. Některé bakterie tvoří bílkoviny z hotových aminokyselin získaných v důsledku vnější výživy, zatímco jiné bakterie samostatně syntetizují aminokyseliny z jednoduchých sloučenin obsahujících dusík a uhlík. Syntéza aminokyselin může být provedena v reakcích aminace, transaminace, amidace a karboxylace. Většina prokaryot je schopna syntetizovat všechny aminokyseliny, které tvoří buněčné proteiny. Charakteristickým rysem biosyntézy aminokyselin je využití běžných biosyntetických drah: cyklus trikarboxylových kyselin, glykolýza, oxidativní pentóza-fosfátová cesta atd. Hlavními výchozími sloučeninami pro syntézu aminokyselin jsou pyruvát a fumarát.
Metabolismus sacharidů liší se mezi autotrofy a heterotrofy (schéma 1). Autotrofní bakterie syntetizují všechny potřebné sacharidy z oxidu uhličitého. Suroviny pro tvorbu sacharidů v heterotrofních bakteriích mohou být: (1) jedno-, dvou- a tříuhlíkové sloučeniny; a (2) polysacharidy (škrob, glykogen, celulóza). K jejich rozkladu má mnoho heterotrofních bakterií exoenzymy (amyláza, pektináza atd.), které hydrolyzují polysacharidy za vzniku glukózy, maltózy, fruktózy atd.
U autotrofních bakterií v Calvinově cyklu vzniká z oxidu uhličitého kyselina ribulóza fosfát-fosforečná-glycerová, která je součástí glykolytických reakcí jdoucích opačným směrem. Konečným produktem reverzní syntézy je glukóza.
Heterotrofní bakterie tvoří glukózu z jedno-, dvou- a tříuhlíkových sloučenin a také je zahrnují do reakce reverzní glykolýzy. Vzhledem k tomu, že některé reakce glykolýzy jsou nevratné, vyvinuly heterotrofní speciální enzymatické reakce, které jim umožňují obejít nevratné reakce katabolické dráhy.
Při rozkladu polysacharidů heterotrofními bakteriemi se výsledné disacharidy dostávají do buněk a pod vlivem maltózy, sacharózy a laktózy podléhají hydrolýze a rozkladu na monosacharidy, které jsou následně fermentovány nebo zahrnuty do interkonverzních reakcí cukrů.
Metabolismus lipidů. Jak exogenní lipidy, tak amfibolity intersticiálního metabolismu mohou sloužit jako výchozí materiály pro tvorbu lipidů v bakteriích. Exogenní lipidy jsou vystaveny působení bakteriálních lipáz a dalších lipolytických enzymů. Mnoho druhů bakterií metabolizuje glycerol, který slouží jako zdroj plastového materiálu a energie. Endogenními zdroji pro syntézu lipidů mohou být acetyl koenzym A, propionyl-ACP, malonyl-ACP (ACP - acetyl transfer protein), fosfodioxyaceton atd.
Výchozím substrátem pro syntézu mastných kyselin se sudým počtem atomů uhlíku je acetylkoenzym A, pro mastné kyseliny s lichým počtem atomů uhlíku - propionyl-ACP a malonyl-ACP. K tvorbě dvojných vazeb v molekule kyseliny u aerobních prokaryot dochází za účasti molekulárního kyslíku a enzymu desaturázy. V anaerobních prokaryotech jsou dvojné vazby zavedeny brzy v syntéze v důsledku dehydratační reakce. Výchozím substrátem pro syntézu fosfolipidů je fosfodioxyaceton (meziprodukt v glykolytické dráze), jehož redukce vede ke vzniku 3-fosforoglycerolu. Ten je pak spojen 2 zbytky mastných kyselin ve formě komplexu s ACP. Produktem reakce je kyselina fosfatidová, jejíž aktivace pomocí CTP a následné přidání serinu, inositolu, glycerolu nebo jiné sloučeniny k fosfátové skupině vede k syntéze odpovídajících fosfolipidů.
Mikroorganismy, které jsou auxotrofní a hypotrofní v mastných kyselinách (například mykoplazmata), je získávají v hotové formě z hostitelských buněk nebo živného média.
Výměna mononukleotidů. Purinové a pyrimidinové mononukleotidy jsou základními složkami DNA a RNA. Mnoho prokaryot je schopno jak používat hotové purinové a pyrimidinové báze, jejich nukleosidy a nukleotidy obsažené v živném médiu, tak je syntetizovat z nízkomolekulárních látek. Bakterie mají enzymy, které katalyzují následující fáze vzájemné přeměny exogenních derivátů purinu a pyrimidinu: dusíkatá báze – nukleosid – nukleotid (mono- – di- – trifosfát).
Syntéza purinových a pyrimidinových mononukleotidů de novo prováděny nezávislými způsoby. Při syntéze purinových nukleotidů v důsledku po sobě jdoucích enzymatických reakcí vzniká kyselina inosinová, ze které se chemickými modifikacemi purinového kruhu syntetizují kyseliny adenylové (AMP) a guanylové (GMP). Syntéza pyrimidinových nukleotidů začíná tvorbou kyseliny orotidylové, jejíž dekarboxylací vzniká kyselina uridylová (UMA). Z posledně jmenovaného vzniká UTP, jehož acylace vede ke vzniku CTP.
Deoxyribonukleotidy vznikají jako výsledek redukce odpovídajících ribonukleotidů na úrovni difosfátů nebo trifosfátů. K syntéze DNA-specifického nukleotidu, kyseliny thymidylové, dochází prostřednictvím enzymatické methylace kyseliny deoxyuridylové.
Iontová výměna. Minerální sloučeniny - ionty, NH 3 +, K +, Mg 2+, Fe 2+, SO 4 2-, PO 4 3- a další bakterie jsou získávány z prostředí jak ve volném stavu, tak ve stavu spojeném s jinými organickými látek. Kationty a anionty jsou do bakteriální buňky transportovány různými způsoby, popsanými v § 3. Rychlost průniku iontů do bakteriální buňky je ovlivněna pH prostředí a fyziologickou aktivitou samotných mikroorganismů.
B) Dýchání bakterií (energetický metabolismus).
Všechny životní procesy jsou energeticky závislé, takže produkce energie je extrémně důležitým aspektem prokaryotického metabolismu. Energii získávají anaerobním a aerobním dýcháním.
Dech nebo biologická oxidace je katabolický proces přenosu elektronů z donorové látky na akceptorovou látku, doprovázený akumulací energie ve vysokoenergetických sloučeninách . Dýchání probíhá procesem katabolických reakcí, v důsledku kterých složité organické látky při rozkladu uvolňují energii a přeměňují se na jednoduché sloučeniny. Energie akumulovaná v makroergických látkách (ATP, GTP, UTP atd.) se využívá při anabolických reakcích.
Podle způsobu dýchání se mikroorganismy dělí na obligátní (přísné) aeroby, obligátní anaeroby A fakultativní anaeroby.
Povinné aeroby potřebují volný kyslík. Donory elektronů v chemoorganotrofních aerobech, které jsou pro člověka patogenní, jsou organické sloučeniny (sacharidy, tuky, bílkoviny) a akceptorem elektronů je molekulární kyslík. K ukládání energie ve formě ATP v chemoorganotrofních aerobech dochází při oxidativní fosforylaci donorů elektronů. Aeroby mají cytochromy (účastní se přenosu elektronů) a také enzymy (kataláza, superoxiddismutáza, peroxidáza), které inaktivují toxické kyslíkové radikály vznikající při dýchání. Superoxiddismutáza inaktivuje nejtoxičtější metabolit, superoxidový radikál v H2O2. Enzym kataláza přeměňuje H 2 O 2 na H 2 O a O 2 .
Zvláštní skupinou aerobů jsou mikroaerofilní bakterie které sice potřebují kyslík k získání energie, ale lépe rostou se zvýšeným obsahem CO 2, např. bakterie rod. Campylobacter A Helicobacter.
Povinné anaeroby nepotřebují volný kyslík, naopak i v malém množství na ně kyslík působí toxicky. Různé organické sloučeniny (hlavně sacharidy) slouží jako donory elektronů pro chemoorganotrofní anaeroby, které jsou pro člověka patogenní. Akceptorem elektronů v chemoorganotrofních anaerobech jsou organické sloučeniny obsahující kyslík - kyseliny nebo ketony, to znamená, že akceptorem elektronů je kyslík vázaný na organický fragment. K ukládání energie v těchto prokaryotech dochází prostřednictvím fosforylace substrátu. Obligátní anaeroby zpravidla nemají cytochromy a enzymy, které inaktivují kyslíkové radikály (negativní kataláza a superoxiddismutáza).
U chemolitotrofních anaerobů, které jsou pro člověka nepatogenní, jsou akceptorem elektronů anorganické sloučeniny obsahující kyslík – dusičnany, sírany, uhličitany.
Zvláštní skupinu anaerobů tvoří aerotolerantní bakterie, které jsou schopny růst v přítomnosti vzdušného kyslíku, ale nevyužívají jej jako akceptor elektronů (například bakterie mléčného kvašení). Aerotolerantní prokaryota jsou pozitivní na katalázu a superoxiddismutázu.
Fakultativní anaeroby jsou schopny existovat v kyslíkovém i bezkyslíkovém prostředí. Jejich donory elektronů jsou organické látky; akceptory elektronů, v závislosti na podmínkách prostředí - molekulární kyslík nebo kyslík vázaný v organických a anorganických sloučeninách. Energii mohou akumulovat fakultativní anaeroby prostřednictvím oxidativní i substrátové fosforylace. Stejně jako aeroby má tato skupina bakterií cytochromy a antioxidační enzymy.
Hlavním substrátem pro výrobu energie jsou sacharidy, které mohou být u chemoheterotrofních prokaryot různých typů dýchání katabolizovány na acetylkoenzym A („aktivovaná kyselina octová“). Lipidy a proteiny mohou působit jako energetické substráty, protože acetylkoenzym A je také jedním z meziproduktů jejich metabolismu (schéma 2).
Katabolismus sacharidů u chemoorganotrofních prokaryot zahrnuje: (a) anaerobní procesy - glykolýzu, pentosafosfátovou dráhu a ketodeoxyfosfoglukonátovou dráhu; b) aerobní proces – cyklus trikarboxylových kyselin (Krebsův cyklus). Anaerobní procesy se vyskytují u všech prokaryot, zatímco aerobní proces je charakteristický pouze pro obligátní aeroby a fakultativní anaeroby. Výroba energie anaerobními cestami je založena na fosforylaci substrátu, zatímco aerobní proces je založen na oxidativní fosforylaci.
Definice pojmů.
Sterilizace, dezinfekce a antiseptika jsou nedílnou součástí moderní lékařské a zejména chirurgické praxe. Pochopení principů a praktické aplikace těchto metod je nezbytné, protože mnoho potenciálně patogenních mikroorganismů může zůstat životaschopných mimo hostitele po dlouhou dobu, vykazují vysokou odolnost vůči fyzikálním a chemickým dezinfekčním prostředkům a jsou relativně snadno přenosné z jedné osoby na druhou.
Antiseptika- ničení nebo zabránění růstu patogenních nebo oportunních mikroorganismů chemickými metodami. Tento termín se obvykle používá k označení vnější aplikace chemického léčiva do živé tkáně.
Antiseptický- látka, která inhibuje růst nebo ničí mikroorganismus (aniž by ovlivnila bakteriální spory). Termín je specifický pro látky, které se používají pro lokální působení na živé tkáně.
Asepse znamená nepřítomnost sepse, ale obecně se tento termín používá pro zdůraznění nepřítomnosti jakýchkoli živých organismů. Aseptické techniky znamená jakýkoli postup určený k likvidaci živých organismů a zabránění jejich opětovné kontaminaci. Moderní chirurgické a mikrobiologické techniky jsou založeny na aseptických postupech.
Biocid- látka hubící všechny živé mikroorganismy, patogenní i nepatogenní, včetně spór.
Biostat- prostředek, který zabraňuje růstu mikroorganismů, ale nemusí je nutně zabíjet.
Dekontaminace- odstranění mikroorganismů bez kvantitativního stanovení. Tento termín je relativní; Konečné odstranění choroboplodných zárodků lze provést sterilizací nebo dezinfekcí.
Dezinfekce- proces, který snižuje počet nebo zcela zničí všechny patogenní mikroorganismy kromě spor.
Germicidní- látka, která ničí mikroorganismy, zejména patogenní. Germicid neničí spory.
Kanalizace- metoda, kterou je mikrobiální kontaminace snížena na „bezpečnou“ úroveň. Tato metoda byla dříve používána k „očištění“ neživých předmětů.
Sterilizace- použití fyzikálních faktorů a (nebo) chemikálií pro úplné zničení nebo zničení všech forem mikrobiálního života.
Sterilizace.
Sterilizace je definována jako zničení nebo odstranění (filtrací) všech mikroorganismů a jejich spor. Sterilizace se obvykle provádí pomocí tepla. Sterilizace, která je jedním z rutinních postupů v provozu mikrobiologické laboratoře, je nezbytnou metodou, jak zajistit, aby kultury, zařízení, sklo a média podporovaly růst pouze nezbytných mikroorganismů, zatímco ostatní mikroby byly zničeny. Existují tyto druhy sterilizace: kalcinace v plameni hořáku, var, působení proudící párou, pára pod tlakem v autoklávu, suché teplo, pasterizace, tindializace, chemická, studená (mechanická) sterilizace.
Výběr metod sterilizace.
Při výběru metod sterilizace je třeba vzít v úvahu následující požadavky:
1. Aktivita: baktericidní, sporicidní, tuberkulocidní, fungicidní a virocidní.
2. Rychlost postupu: sterilizace by měla být provedena co nejrychleji.
3. Propustnost: sterilizační látky musí proniknout přes obal a do vnitřních částí nástroje.
4. Kompatibilita: Nemělo by docházet k žádné změně ve struktuře nebo funkci materiálů, které jsou několikrát sterilizovány.
5. Netoxický: nemělo by existovat žádné ohrožení lidského zdraví nebo životního prostředí.
6. Stabilita organického materiálu: Účinnost sterilizace by neměla být narušena přítomností organického materiálu.
7. Adaptabilita: možnost použití pro velké i malé objemy sterilizovaného materiálu.
8. Kontrola v průběhu času: Cyklus zpracování musí být snadno a přesně kontrolován.
9. Cena: přiměřené náklady na vybavení, instalaci a provoz.
 Fyzikální sterilizátory
Fyzikální sterilizátory
Mokrý teplý, který vzniká během procesu parního autoklávování, je hlavním sterilizačním činidlem používaným v laboratořích klinické mikrobiologie. Autoklávy se používají ke sterilizaci kultivačních médií, tepelně odolných materiálů a zpracování infekčního odpadu. Parní sterilizátor nebo autokláv je izolovaná tlaková komora, která využívá nasycenou páru k vytvoření vysokých teplot (obrázek 1). Vzduch je z komory odstraněn vytlačením hmoty nebo vytvořením vakua. Nejčastěji používanými autoklávy jsou hromadná substituce. Lehčí pára se uvolňuje do komory, aby vytlačila těžší vzduch. Krátké ošetření tlakovou párou může zničit bakteriální spory. Pro běžnou sterilizaci kultivačních médií a dalších materiálů je doba expozice 15 minut při 121ºC a tlak je 1,5 kg na 1 centimetr čtvereční. U infekčního odpadu se doba expozice zvyšuje na 30-60 minut. Kromě správného času a teploty je při sterilizaci velmi důležitý přímý kontakt s párou. Při zpracování infekčního materiálu by mělo být zajištěno maximální pronikání páry do odpadu. Takový materiál musí být zpracován při teplotě 132ºС. Antineoplastická léčiva, toxické chemikálie a radioizotopy, které se nemusí rozkládat, a nestabilní chemikálie, které se mohou odpařovat a šířit v komoře vlivem tepla, by neměly být autoklávovány.
 Sterilizace suchým teplem používá se pro materiály, které nelze sterilizovat párou kvůli možnosti poškození nebo kvůli nepropustnosti materiálu pro páru. Suché teplo je méně účinné než vlhké teplo a vyžaduje delší dobu působení a vyšší teploty. Sterilizace suchým teplem se obvykle provádí v peci se suchým teplem (obr. 2). Mechanismus sterilizace suchým teplem je oxidační proces. Příklady materiálů, které používají sterilizaci suchým teplem, zahrnují oleje, prášky, ostré nástroje a skleněné nádobí. Jako alternativní metody zpracování infekčního odpadu se používá suché teplo nebo tepelná inaktivace-sterilizace.
Sterilizace suchým teplem používá se pro materiály, které nelze sterilizovat párou kvůli možnosti poškození nebo kvůli nepropustnosti materiálu pro páru. Suché teplo je méně účinné než vlhké teplo a vyžaduje delší dobu působení a vyšší teploty. Sterilizace suchým teplem se obvykle provádí v peci se suchým teplem (obr. 2). Mechanismus sterilizace suchým teplem je oxidační proces. Příklady materiálů, které používají sterilizaci suchým teplem, zahrnují oleje, prášky, ostré nástroje a skleněné nádobí. Jako alternativní metody zpracování infekčního odpadu se používá suché teplo nebo tepelná inaktivace-sterilizace.
Pasterizace ničí patogenní mikroorganismy rychlým zahřátím látky na 71,1ºC po dobu 15 sekund a následným rychlým ochlazením. Pasterizace není sterilizace, protože ne všechny mikroorganismy jsou na ni citlivé. Tato metoda eliminovala potravinovou cestu přenosu nemocí, jako je tuberkulóza trávicího traktu a Q-horečka.
Tyndalizace je metoda přerušované tepelné sterilizace, kterou lze použít k usmrcení všech bakterií v roztocích. Vzhledem k tomu, že rostoucí bakterie jsou snadno zabity krátkým varem (5krát po dobu 1 hodiny po dobu 5 minut), vše, co je třeba udělat, je nechat roztok po určitou dobu odstát, než teplo naruší dozrávání spor s výraznou ztrátou. jejich odolnosti vůči teplu.
Filtrace je proces používaný k odstranění choroboplodných zárodků a mikroskopických částí z roztoků, vzduchu a jiných plynů. Nejběžnější použití sterilizace filtrací v laboratoři je pro zpracování diagnostických přípravků, kultivačních médií, médií pro tkáňové kultury, sér a roztoků, které obsahují složky séra. Další běžnou aplikací filtrace je sterilizace vzduchu a plynů. Plastové nebo papírové membránové filtry, které se liší průměrem pórů (cca 12 až 0,22 μm) a používají se k mechanické separaci, slouží také ke sběru mikrobů z kapalin pro mikroskopické vyšetření nebo kultivaci přímo na filtru, když je umístěn na povrchově impregnovanou živinu střední.
Ultrafialové záření je druh záření elektromagnetických vln, které působí na buněčnou nukleovou kyselinu. Mikroorganismy jsou vysoce citlivé na ultrafialové paprsky o vlnové délce 254 nm. Ultrafialové světlo se nejvíce používá k ničení mikroorganismů ve vzduchu nebo na jakémkoli povrchu. Další aplikace jsou studená sterilizace určitých chemikálií a plastů pro farmaceutické účely, sterilizace séra pro buněčné kultury a dezinfekce vody. Významnou nevýhodou ultrafialového záření jako sterilizátoru je jeho neschopnost pronikat materiály.
Ionizující radiace v elektromagnetickém spektru má smrtelný účinek na mikroorganismy. Toto spektrum zahrnuje mikrovlny, gama záření, rentgenové záření a tok elektronů. Smrtící účinek ionizujícího záření nastává v důsledku přímého účinku na cílovou molekulu, což má za následek přenos energie do molekuly; a v důsledku nepřímého působení – difúze radikálů.
Ultrazvuková energie inaktivuje mikroorganismy ve vodných roztocích s nízkou frekvencí. K fyzikálnímu účinku sonikace dochází v důsledku kavitace. Ultrazvukové čističe a další zařízení se často používají k čištění nástrojů, ale nejsou považovány za sterilizační prostředky. Kombinace ultrazvuku s chemickým ošetřením však mikroorganismy zabíjí.
Chemické sterilizátory
2 % glutaraldehyd Jako kapalný chemický sterilizační prostředek byl dříve široce používán ke zpracování lékařských a chirurgických materiálů, které nelze sterilizovat teplem nebo zářením. Glutaraldehyd se také používá při přípravě vakcín.
Dezinfekce.
Dezinfekce může být provedena chemickými metodami nebo varem. Var je účinný způsob dezinfekce zařízení, jako jsou jehly a stříkačky, pokud není k dispozici autokláv. Předčištěné lékařské nástroje by se měly vařit po dobu 20 minut. Chemická dezinfekce se používá pro zařízení citlivá na teplo, která mohou být poškozena vysokou teplotou. Chemické dezinfekční prostředky, jako jsou chlórové složky, ethyl a isopropylalkohol, kvartérní amoniové složky a glutaraldehyd, jsou široce používány.
Chemické dezinfekční prostředky.
Alkohol (ethyl a isopropyl), rozpuštěný ve vodě na koncentraci 60-85%, je velmi účinný při dezinfekci. Alkoholy mají baktericidní, fungicidní a tuberkulocidní účinky, ale neovlivňují spory. Ethylalkohol má širší spektrum virocidní aktivity než isopropylalkohol, takže je účinnější proti lipofilním a hydrofilním virům.
Řešení 37 % formaldeide, který se nazývá formalín, lze použít jako sterilizátor, zatímco jeho koncentrace 3-8% lze použít jako dezinfekční prostředek.
fenol v čisté formě se nepoužívá jako dezinfekční prostředek pro svou toxicitu, schopnost vyvolat rozvoj nádorů a korozi. Jako dezinfekční prostředky se široce používají deriváty fenolu, ve kterých funkční skupina (chlor, brom, alkyl, benzyl, fenyl, amyl) nahrazuje jeden z atomů vodíku v aromatickém kruhu. Taková substituce snižuje nevýhody fenolu. Fenolové složky zabíjejí mikroby inaktivací enzymatických systémů, precipitací proteinů a narušením buněčné stěny a membrány. Obvykle se používají koncentrace 2-5 %, přičemž nižší koncentrace vyžadují delší dobu expozice.
Halogeny. K dezinfekci v laboratorní praxi se používá pouze chlór a jód. Protože chlor je silné oxidační činidlo, má se za to, že zabíjí mikroby oxidací. Předpokládá se, že jód zabíjí mikroorganismy reakcí s N-H a S-H skupinami aminokyselin, stejně jako s fenolovou skupinou aminokyseliny tyrosinu a dvojnými vazbami uhlík-uhlík nenasycených mastných kyselin. Konvenční ošetření zahrnuje rozprašování 2-5% roztoku formaldehydu v přítomnosti páry o teplotě 60-80ºC.
Antiseptický.
Antiseptika lze nalézt v mikrobiologických laboratořích, především v látkách používaných k mytí rukou. Když zdravotnický personál poskytuje pacientům neodkladnou péči pomocí látek obsahujících antibakteriální látky, snižuje se tím počet infekcí získaných v nemocnici. Nejběžnější chemikálie nacházející se v mycích prostředcích jsou alkoholy, chlorhexidin glukonát, jodofory, chloroxylenol a triclosan.
Tradičními metodami nakládání s odpady a odpadky jsou spalování a parní sterilizace.
Hořící je metoda volby pro zpracování odpadu a suti. Tato metoda činí odpad neinfekčním a také mění svůj tvar a velikost. Sterilizace je účinný způsob úpravy odpadu, který však nemění jeho tvar. Parní sterilizace v autoklávu při 121ºC po dobu minimálně 15 minut zničí všechny formy mikrobiálního života, včetně velkého množství bakteriálních spor. Tento typ kompletní sterilizace lze také provést suchým teplem při teplotě 160-170ºC po dobu 2-4 hodin. Měli byste však zajistit, aby suché teplo bylo v kontaktu s materiálem, který má být sterilizován. Lahve, které obsahují tekutinu, proto musí být volně uzavřeny zátkami nebo vatovými tampony, aby se pára a teplo mohly vyměňovat se vzduchem v lahvích. Nádoby na biologické nebezpečí obsahující odpad by měly být těsně uzavřeny. Sterilizovaný biologicky nebezpečný materiál by měl být uzavřen ve vhodných označených nádobách.
Sterilizace párou (autokláv). Infekční zbytky se považují za dekontaminované, když se počet vegetativních bakterií, hub, mykobakterií a virů obsahujících lipidy sníží 6 lgkrát a bakteriální endospory se sníží 4 lgkrát.
Výživa bakterií.
Výživa. Výživa bakteriální buňky by měla být chápána jako proces absorpce a asimilace plastového materiálu a energie v důsledku transformačních reakcí. . Výživové typy prokaryot jsou komplexní a rozmanité. Liší se v závislosti na způsobu vstupu živin do bakteriální buňky, zdrojích uhlíku a dusíku, způsobu získávání energie a povaze donorů elektronů.
Transport živin do buňky může být prováděna 3 mechanismy: pasivní difúzí, facilitovanou difúzí a aktivním transportem.
Pasivní difúze je nespecifický energeticky závislý proces probíhající podél koncentračního gradientu látek (látka z média s vyšší koncentrací pasivně podle zákonů osmózy vstupuje do média s nižší koncentrací). Pasivní difúzí se do bakteriální buňky dostává omezené množství látek, některé ionty a monosacharidy. Rychlost přenosu látky při pasivní difúzi je nevýznamná a závisí na lipofilitě a velikosti transportovaných molekul.
Usnadněná difúze je energeticky nezávislý transport látek po koncentračním gradientu pomocí enzymů permeázy. Permeázy jsou specifické membránové proteiny, které usnadňují průchod látek přes cytoplazmatickou membránu. Permeáza na sebe fixuje molekulu transportované látky, společně s ní prochází cytoplazmatickou membránou, načež se komplex „látka-permeáza“ disociuje. Uvolněná permeáza se používá k přenášení dalších molekul. U prokaryot vstupuje do buňky pouze glycerol usnadněnou difúzí. V tomto případě intracelulární koncentrace glycerolu odpovídá koncentraci mimo buňku. Usnadněná difúze je nejcharakterističtější pro eukaryotické mikroorganismy.
Aktivní transport- Jedná se o energeticky závislý přenos látek do buňky proti koncentračnímu gradientu pomocí specifických enzymů. Naprostá většina látek (ionty, sacharidy, aminokyseliny, lipidy atd.) vstupuje do bakteriální buňky aktivním transportem. K aktivnímu transportu může dojít: (1) bez chemické modifikace přepravované látky; (2) s chemickou modifikací.
Jaké bakterie existují: typy bakterií, jejich klasifikace
Bakterie jsou drobné mikroorganismy, které se objevily před mnoha tisíci lety. Mikroby není možné vidět pouhým okem, ale neměli bychom zapomínat na jejich existenci. Existuje obrovské množství bacilů. Jejich klasifikací, studiem, odrůdami, strukturními znaky a fyziologií se zabývá věda mikrobiologie.
Mikroorganismy se nazývají různě, v závislosti na typu jejich působení a funkce. Pod mikroskopem můžete pozorovat, jak se tito malí tvorové vzájemně ovlivňují. První mikroorganismy byly svou formou dosti primitivní, ale jejich význam by v žádném případě neměl být podceňován. Od samého počátku se bacily vyvíjely, vytvářely kolonie a snažily se přežít v měnících se klimatických podmínkách. Různé vibria jsou schopny vyměňovat si aminokyseliny, aby mohly normálně růst a vyvíjet se.
Dnes je těžké říci, kolik druhů těchto mikroorganismů je na zemi (toto číslo přesahuje milion), ale ty nejznámější a jejich jména zná téměř každý člověk. Nezáleží na tom, jaký druh mikrobů existuje nebo jak se jmenují, všichni mají jednu výhodu - žijí v koloniích, což jim usnadňuje adaptaci a přežití.
Nejprve pojďme zjistit, jaké mikroorganismy existují. Nejjednodušší klasifikace je dobrá a špatná. Jinými slovy, ty, které lidskému tělu škodí, způsobují mnoho nemocí a ty, které jsou prospěšné. Dále si podrobně povíme, jaké jsou hlavní prospěšné bakterie a uvedeme jejich popis.

Mikroorganismy můžete také klasifikovat podle jejich tvaru a vlastností. Pravděpodobně si mnozí pamatují, že ve školních učebnicích byla speciální tabulka zobrazující různé mikroorganismy a vedle nich byl význam a jejich role v přírodě. Existuje několik typů bakterií:
- koky - malé kuličky, které připomínají řetěz, protože jsou umístěny jeden po druhém;
- tyčovitý;
- spirilla, spirochety (mají svinutý tvar);
- vibrace.
Bakterie různých tvarů
Již jsme zmínili, že jedna z klasifikací rozděluje mikroby na typy v závislosti na jejich formách.
Bakterie Bacillus mají také některé vlastnosti. Existují například tyčovité typy se špičatými kůly, zesílenými, zaoblenými nebo rovnými konci. Tyčinkovité mikroby jsou zpravidla velmi rozdílné a jsou neustále v chaosu, neseřazují se v řetězci (s výjimkou streptobacilů) a neulpívají na sobě (kromě diplobacilů).
Mezi sférické mikroorganismy mikrobiologové řadí streptokoky, stafylokoky, diplokoky a gonokoky. Mohou to být páry nebo dlouhé řetězce kuliček.
Zakřivené bacily jsou spirilla, spirochéty. Jsou vždy aktivní, ale neprodukují spory. Spirilla je bezpečná pro lidi i zvířata. Spirilu od spirochet rozeznáte, pokud si dáte pozor na počet přeslenů, jsou méně svinuté a mají na končetinách zvláštní bičíky.
Druhy patogenních bakterií
Například skupina mikroorganismů zvaných koky, konkrétněji streptokoky a stafylokoky, se stávají původci skutečných hnisavých onemocnění (furunkulóza, streptokoková angína).
Anaeroby žijí a vyvíjejí se dobře bez kyslíku pro některé typy těchto mikroorganismů se kyslík stává osudným. Aerobní mikrobi potřebují ke svému růstu kyslík.
Archaea jsou prakticky bezbarvé jednobuněčné organismy.
Musíte si dávat pozor na patogenní bakterie, protože způsobují infekce, jsou považovány za odolné vůči protilátkám. Existuje mnoho informací o půdě, hnilobných mikroorganismech, které mohou být škodlivé nebo prospěšné.

Obecně platí, že spirilla nejsou nebezpečné, ale některé druhy mohou způsobit sodoku.
Druhy prospěšných bakterií
I školáci vědí, že bacil může být užitečný i škodlivý. Lidé znají některá jména z doslechu (stafylokok, streptokok, morový bacil). Jde o škodlivé tvory, kteří zasahují nejen do vnějšího prostředí, ale i do člověka. Existují mikroskopické bacily, které způsobují otravu jídlem.
Určitě potřebujete znát užitečné informace o kyselině mléčné, potravinách a probiotických mikroorganismech. Například probiotika, jinými slovy dobré organismy, se často používají pro lékařské účely. Můžete se zeptat: za co? Neumožňují množení škodlivých bakterií uvnitř člověka, posilují ochranné funkce střev, mají dobrý vliv na imunitní systém člověka.
Bifidobakterie jsou také velmi prospěšné pro střeva. Vibria kyseliny mléčné zahrnují asi 25 druhů. V lidském těle se nacházejí v obrovském množství, ale nejsou nebezpečné. Naopak chrání gastrointestinální trakt před hnilobnými a jinými mikroby.
Když už jsme u těch dobrých, nelze nezmínit obrovské druhy streptomycet. Jsou známy těm, kteří užívali chloramfenikol, erytromycin a podobné léky.
Existují mikroorganismy, jako je Azotobacter. Žijí v půdě řadu let, působí příznivě na půdu, stimulují růst rostlin, čistí půdu od těžkých kovů. Jsou nepostradatelné v lékařství, zemědělství, lékařství a potravinářském průmyslu.
Typy bakteriální variability
Mikrobi jsou ze své podstaty velmi nestálí, rychle umírají, mohou být spontánní nebo indukovaní. Nebudeme se podrobně zabývat variabilitou bakterií, protože tyto informace jsou zajímavější pro ty, kteří se zajímají o mikrobiologii a všechna její odvětví.
Druhy bakterií pro septiky
Obyvatelé soukromých domů chápou naléhavou potřebu čištění odpadních vod, stejně jako žumpy. Dnes můžete rychle a efektivně vyčistit odtoky pomocí speciálních bakterií pro septiky. To je pro člověka obrovská úleva, protože čištění kanalizací není příjemný úkol.
Již jsme si ujasnili, kde se biologické čištění odpadních vod používá, a nyní si povíme o systému samotném. Bakterie pro septiky se pěstují v laboratořích, zabíjejí nepříjemný zápach odpadních vod, dezinfikují drenážní studny, žumpy, snižují objem odpadních vod. Existují tři typy bakterií, které se používají pro septiky:
- aerobní;
- anaerobní;
- živé (bioaktivátory).

Lidé velmi často používají kombinované metody čištění. Přísně dodržujte pokyny na produktu a ujistěte se, že hladina vody přispívá k normálnímu přežití bakterií. Nezapomeňte také použít drenáž alespoň jednou za dva týdny, abyste měli bakterie co jíst, jinak zemřou. Nezapomeňte, že chlór z čisticích prášků a kapalin zabíjí bakterie.
Nejoblíbenější bakterie jsou Doctor Robic, Septifos, Waste Treat.
Druhy bakterií v moči
Teoreticky by v moči neměly být žádné bakterie, ale po různých akcích a situacích se drobné mikroorganismy usazují, kde chtějí: ve vagíně, v nose, ve vodě a tak dále. Pokud jsou během testů zjištěny bakterie, znamená to, že osoba trpí onemocněním ledvin, močového měchýře nebo močovodů. Existuje několik způsobů, jak se mikroorganismy dostávají do moči. Před léčbou je velmi důležité vyšetřit a přesně určit typ bakterie a cestu vstupu. To lze zjistit biologickou kultivací moči, kdy jsou bakterie umístěny v příznivém prostředí. Dále se kontroluje reakce bakterií na různá antibiotika.
Přejeme vám, abyste byli vždy zdraví. Dávejte na sebe pozor, myjte si pravidelně ruce, chraňte své tělo před škodlivými bakteriemi!
2.1. Systematika a nomenklatura mikrobů
Mikrobiální svět lze rozdělit na buněčnou a nebuněčnou formu. Buněčné formy mikrobů představují bakterie, houby a prvoci. Mohou být nazývány mikroorganismy. Nebuněčné formy představují viry, viroidy a priony.
Nová klasifikace buněčných mikrobů zahrnuje následující taxonomické jednotky: domény, říše, typy, třídy, řády, čeledi, rody, druhy. Klasifikace mikroorganismů je založena na jejich genetické příbuznosti a také na morfologických, fyziologických, antigenních a molekulárně biologických vlastnostech.
Viry se často nepovažují za organismy, ale za autonomní genetické struktury, takže budou posuzovány samostatně.
Buněčné formy mikrobů jsou rozděleny do tří domén. domény Bakterie A Archaebakterie zahrnují mikroby s prokaryotickým typem buněčné struktury. Zástupci domény Eukarya jsou eukaryota. Skládá se ze 4 království:
Houbová království (Houby, Eumycota);
říše prvoků (Protozoa);
království Chromista(chrom);
Mikrobi s nespecifikovanou taxonomickou pozicí (Mikrospora, mikrosporidie).
Rozdíly v organizaci prokaryotických a eukaryotických buněk jsou uvedeny v tabulce. 2.1.
Tabulka 2.1. Známky prokaryotické a eukaryotické buňky
2.2. Klasifikace a morfologie bakterií
Výraz "bakterie" pochází ze slova bakterie, co znamená hůl? Bakterie jsou prokaryota. Jsou rozděleny do dvou domén: Bakterie A Archaebakterie. Bakterie zahrnuté v doméně archaebakterie, představují jednu z nejstarších forem života. Mají strukturní rysy buněčné stěny (chybí jim peptidoglykan) a ribozomální RNA. Nejsou mezi nimi patogeny infekčních chorob.
V rámci domény jsou bakterie rozděleny do následujících taxonomických kategorií: třída, kmen, řád, čeleď, rod, druh. Jednou z hlavních taxonomických kategorií je druh. Druh je soubor jedinců stejného původu a genotypu, které spojují podobné vlastnosti, které je odlišují od ostatních zástupců rodu. Druhové jméno odpovídá binární nomenklatuře, tzn. se skládá ze dvou slov. Například původce záškrtu se píše jako Corynebacterium diphtheriae. První slovo je název rodu a píše se s velkým písmenem, druhé slovo označuje druh a píše se s malým písmenem.
Při opětovném zmínce o druhu se rodové jméno zkrátí na počáteční písmeno, např. C. diphtheriae.
Soubor homogenních mikroorganismů izolovaných na živném médiu, vyznačujících se podobnými morfologickými, tinctoriálními (vztah k barvivům), kulturními, biochemickými a antigenními vlastnostmi, je tzv. čistá kultura.Čistá kultura mikroorganismů izolovaná ze specifického zdroje a odlišná od ostatních členů druhu se nazývá kmen. Blízký pojmu „kmen“ je pojem „klon“. Klon je soubor potomků vyrostlých z jedné mikrobiální buňky.
Pro označení určitých souborů mikroorganismů, které se liší v určitých vlastnostech, se používá přípona „var“ (odrůda), proto se mikroorganismy podle povahy odlišností označují jako morfovary (rozdíl v morfologii), rezistentní produkty (rozdíl v rezistenci). například na antibiotika), sérovary (rozdíl v antigenech), fagovary (rozdíl v citlivosti na bakteriofágy), biovary (rozdíl v biologických vlastnostech), chemovary (rozdíl v biochemických vlastnostech) atd.
Dříve byla základem pro klasifikaci bakterií strukturální rys buněčné stěny. Rozdělení bakterií podle strukturních znaků buněčné stěny je spojeno s možnou variabilitou jejich zbarvení v té či oné barvě pomocí Gramovy metody. Podle této metody navržené v roce 1884 dánským vědcem H. Gramem se v závislosti na výsledcích barvení rozdělují bakterie na grampozitivní, zbarvené modrofialově a gramnegativní, zbarvené červeně.
V současné době je klasifikace založena na stupni genetické příbuznosti, na základě studia struktury genomu ribozomální RNA (rRNA) (viz kapitola 5), stanovení procenta guaninových cytosinových párů (GC párů) v genomu, sestrojení a restrikční mapu genomu a studium stupně hybridizace. Zohledňují se také fenotypové ukazatele: postoj k barvení podle Grama, morfologické, kulturní a biochemické vlastnosti, antigenní struktura.
Doména Bakterie zahrnuje 23 typů, z nichž následující mají lékařský význam.
Většina gramnegativních bakterií je seskupena do kmene Proteobakterie(pojmenovaný po řeckém bohu Proteus, schopný nabývat různých podob). Typ Proteobakterie rozdělena do 5 tříd:
Třída Alfaproteobakterie(narození Rickettsia, Orientia, Erlichia, Bartonella, Brucella);
Třída Betaproteobakterie(narození Bordetella, Burholderia, Neisseria, Spirillum);
Třída Gamaproteobakterie(zástupci rodiny Enterobacteriaceae porod Francisella, Legionella, Coxiella, Pseudomonas, Vibrio);
Třída Deltaproteobakterie(rod Bilophila);
Třída Epsilonproteobakterie(narození Campilobacter, Helicobacter). Gramnegativní bakterie také zahrnují následující typy:
typ Chlamydie(narození Chlamydie, Chlamydophila), typ Spirochaetes(narození Spirocheta, Borrelia, Treponema, Leptospira); typ Bacteroides(narození Bacteroides, Prevotella, Porphyromonas).
Gram-pozitivní bakterie se vyskytují v následujících typech:
Typ Firmicutes zahrnuje třídu Clostridium(narození Clostridium, Peptococcus), Třída Bacily (Listeria, Staphylococcus, Lactobacillus, Streptococcus) a třída Mollicutes(narození mykoplazma, ureaplazma), což jsou bakterie, které nemají buněčnou stěnu;
typ Aktinobakterie(narození Actinomyces, Micrococcus, Corynebacterium, Mycobacterium, Gardnerella, Bifidobacterium, Propionibacterium, Mobiluncus).
2.2.1. Morfologické formy bakterií
Existuje několik hlavních forem bakterií: kokoidní, tyčinkovité, svinuté a větvené (obr. 2.1).
Kulovité formy nebo koky- kulovité bakterie o velikosti 0,5-1 mikronu, které se podle vzájemné polohy dělí na mikrokoky, diplokoky, streptokoky, tetrakoky, sarciny a stafylokoky.
Mikrokoky (z řečtiny. mikros- malé) - samostatně umístěné buňky.
Diplococcus (z řečtiny. diploos- dvojité), nebo párové koky, jsou umístěny v párech (pneumokok, gonokok, meningokok), protože buňky se po rozdělení neoddělují. Pneumokok (původce zápalu plic) má na opačných stranách kopinatý tvar a gonokok (původce kapavky) a meningokok (původce
 Rýže. 2.1. Tvary bakterií
Rýže. 2.1. Tvary bakterií
původce epidemické meningitidy) mají tvar kávových zrn s konkávním povrchem obráceným k sobě.
Streptokoky (z řečtiny. streptos- řetězec) - buňky kulatého nebo protáhlého tvaru, které tvoří řetězec v důsledku buněčného dělení ve stejné rovině a udržují spojení mezi nimi v místě dělení.
Sarcins (z lat. sarcina- trs, balík) jsou uspořádány ve formě balíčků po 8 nebo více kokech, protože vznikají při buněčném dělení ve třech vzájemně kolmých rovinách.
Stafylokoky (z řečtiny. stafyle- hroznový hrozen) - koky umístěné ve formě trsu hroznů v důsledku dělení v různých rovinách.
Tyčinkovité bakterie se liší velikostí, tvarem konců buněk a vzájemnou polohou buněk. Délka buňky je 1-10 µm, tloušťka 0,5-2 µm. Tyčinky mohou mít pravdu
(Escherichia coli aj.) a nepravidelný kyjovitý (Corynebacteria aj.) tvar. Mezi nejmenší tyčinkovité bakterie patří rickettsie.
Konce tyčinek mohou být odříznuté (anthrax bacillus), zaoblené (Escherichia coli), špičaté (fusobakterie) nebo ve formě ztluštění. V druhém případě vypadá tyč jako kyj (Corynebacterium diphtheria).
Mírně zakřivené tyčinky se nazývají vibrios (Vibrio cholerae). Většina tyčinkovitých bakterií je uspořádána náhodně, protože buňky se po rozdělení od sebe vzdalují. Pokud buňky po dělení zůstanou spojeny společnými úlomky buněčné stěny a nerozcházejí se, pak jsou umístěny vůči sobě pod úhlem (Corynebacterium diphtheria) nebo tvoří řetězec (bacil antraxu).
Zkroucené tvary- spirálovité bakterie, které se vyskytují ve dvou typech: spirilla a spirochety. Spirilly mají vzhled svinutých buněk ve tvaru vývrtky s velkými kadeřemi. Mezi patogenní spirilly patří původce sodoku (nemoc z kousnutí potkanem), dále kampylobakter a helicobacter, které mají křivky připomínající křídla létajícího racka. Spirochety jsou tenké, dlouhé, spletité bakterie, které se liší od spirilly menšími kadeřemi a vzorem pohybu. Zvláštnosti jejich struktury jsou popsány níže.
Větvení - tyčinkovité bakterie, které mohou mít větve ve tvaru Y nalezené u bifidobakterií, mohou být také prezentovány ve formě vláknitých rozvětvených buněk, které se mohou proplétat a vytvářet mycelium, jak bylo pozorováno u aktinomycet.
2.2.2. Struktura bakteriální buňky
Struktura bakterií byla dobře studována pomocí elektronové mikroskopie celých buněk a jejich ultratenkých řezů, stejně jako jinými metodami. Bakteriální buňka je obklopena membránou skládající se z buněčné stěny a cytoplazmatické membrány. Pod skořápkou se nachází protoplazma, skládající se z cytoplazmy s inkluzemi a dědičného aparátu - obdoba jádra, zvaného nukleoid (obr. 2.2). Existují další struktury: kapsle, mikrokapsle, hlen, bičíky, pili. Některé bakterie jsou schopny tvořit spory za nepříznivých podmínek.
 Rýže. 2.2. Struktura bakteriální buňky: 1 - pouzdro; 2 - buněčná stěna; 3 - cytoplazmatická membrána; 4 - mesozomy; 5 - nukleoid; 6 - plazmid; 7 - ribozomy; 8 - inkluze; 9 - bičík; 10 - pili (klky)
Rýže. 2.2. Struktura bakteriální buňky: 1 - pouzdro; 2 - buněčná stěna; 3 - cytoplazmatická membrána; 4 - mesozomy; 5 - nukleoid; 6 - plazmid; 7 - ribozomy; 8 - inkluze; 9 - bičík; 10 - pili (klky)
Buněčná stěna- silná, elastická struktura, která dává bakterii určitý tvar a spolu s pod ní ležící cytoplazmatickou membránou omezuje vysoký osmotický tlak v bakteriální buňce. Podílí se na procesu buněčného dělení a transportu metabolitů, má receptory pro bakteriofágy, bakteriociny a různé látky. Nejtlustší buněčná stěna se nachází u grampozitivních bakterií (obr. 2.3). Pokud je tedy tloušťka buněčné stěny gramnegativních bakterií asi 15-20 nm, pak u grampozitivních bakterií může dosáhnout 50 nm nebo více.
Základem bakteriální buněčné stěny je peptidoglykan. Peptidoglykan je polymer. Představují ho paralelní polysacharidové glykanové řetězce sestávající z opakujících se zbytků N-acetylglukosaminu a N-acetylmuramové kyseliny spojených glykosidickou vazbou. Tato vazba je narušena lysozymem, což je acetylmuramidáza.
Tetrapeptid je navázán na kyselinu N-acetylmuramovou kovalentními vazbami. Tetrapeptid se skládá z L-alaninu, který je spojen s kyselinou N-acetylmuramovou; D-glutamin, který je u grampozitivních bakterií kombinován s L-lysinem a u gram-tri-
 Rýže. 2.3. Schéma architektury bakteriální buněčné stěny
Rýže. 2.3. Schéma architektury bakteriální buněčné stěny
prospěšné bakterie - s kyselinou diaminopimelovou (DAP), která je prekurzorem lysinu v procesu bakteriální biosyntézy aminokyselin a je jedinečnou sloučeninou přítomnou pouze v bakteriích; 4. aminokyselinou je D-alanin (obr. 2.4).
Buněčná stěna grampozitivních bakterií obsahuje malé množství polysacharidů, lipidů a proteinů. Hlavní složkou buněčné stěny těchto bakterií je vícevrstvý peptidoglykan (murein, mukopeptid), tvořící 40-90 % hmoty buněčné stěny. Tetrapeptidy různých vrstev peptidoglykanu v grampozitivních bakteriích jsou navzájem spojeny polypeptidovými řetězci 5 glycinových zbytků (pentaglycin), což dává peptidoglykanu pevnou geometrickou strukturu (obr. 2.4, b). Kovalentně spojen s peptidoglykanem buněčné stěny grampozitivních bakterií teichoové kyseliny(z řečtiny techhos- stěna), jejíž molekuly jsou řetězce 8-50 glycerolových a ribitolových zbytků spojených fosfátovými můstky. Tvar a síla bakterií je dána tuhou vláknitou strukturou vícevrstvého peptidoglykanu, s příčnými vazbami peptidů.
 Rýže. 2.4. Struktura peptidoglykanu: a - gramnegativní bakterie; b - grampozitivní bakterie
Rýže. 2.4. Struktura peptidoglykanu: a - gramnegativní bakterie; b - grampozitivní bakterie
Schopnost grampozitivních bakterií zadržet genciánovou violeť v kombinaci s jódem při barvení pomocí Gramova barviva (modrofialová barva bakterií) je spojena s vlastností vícevrstvého peptidoglykanu interagovat s barvivem. Navíc následné ošetření bakteriálního nátěru alkoholem způsobí zúžení pórů v peptidoglykanu a tím zadrží barvivo v buněčné stěně.
Gramnegativní bakterie po působení alkoholu ztrácejí barvivo, což je způsobeno menším množstvím peptidoglykanu (5-10 % hmoty buněčné stěny); odbarvují se alkoholem a při ošetření fuchsinem nebo safraninem zčervenají. To je způsobeno strukturálními rysy buněčné stěny. Peptidoglykan v buněčné stěně gramnegativních bakterií je zastoupen 1-2 vrstvami. Tetrapeptidy vrstev jsou navzájem spojeny přímou peptidovou vazbou mezi aminoskupinou DAP jednoho tetrapeptidu a karboxylovou skupinou D-alaninu tetrapeptidu další vrstvy (obr. 2.4, a). Mimo peptidoglykan je vrstva lipoprotein, připojen k peptidoglykanu přes DAP. Následován vnější membrána buněčná stěna.
Vnější membrána je mozaiková struktura složená z lipopolysacharidů (LPS), fosfolipidů a proteinů. Jeho vnitřní vrstva je reprezentována fosfolipidy a vnější vrstva obsahuje LPS (obr. 2.5). Vnější paměť tedy
 Rýže. 2.5. Struktura lipopolysacharidů
Rýže. 2.5. Struktura lipopolysacharidů
brána je asymetrická. Vnější membrána LPS se skládá ze tří fragmentů:
Lipid A má konzervativní strukturu, téměř stejnou u gramnegativních bakterií. Lipid A se skládá z fosforylovaných glukosaminových disacharidových jednotek, ke kterým jsou připojeny dlouhé řetězce mastných kyselin (viz obr. 2.5);
Jádro nebo jádrová část kůry (z lat. jádro- jádro), relativně konzervativní oligosacharidová struktura;
Vysoce variabilní O-specifický polysacharidový řetězec vytvořený opakováním identických oligosacharidových sekvencí.
LPS je ukotven ve vnější membráně lipidem A, který způsobuje toxicitu LPS, a proto je identifikován s endotoxinem. Zničení bakterií antibiotiky vede k uvolnění velkého množství endotoxinu, který může u pacienta způsobit endotoxický šok. Jádro nebo jádrová část LPS sahá od lipidu A. Nejkonstantnější částí jádra LPS je kyselina ketodeoxyoktonová. O-specifický polysacharidový řetězec vycházející z jádra molekuly LPS,
sestávající z opakujících se oligosacharidových jednotek, určuje séroskupinu, sérovar (typ bakterie detekovaný pomocí imunitního séra) konkrétního kmene bakterií. Pojem LPS je tedy spojen s pojmem O-antigen, pomocí kterého lze diferencovat bakterie. Genetické změny mohou vést k defektům, zkrácení bakteriálního LPS a v důsledku toho ke vzniku hrubých kolonií R-forem, které ztrácejí specificitu O-antigenu.
Ne všechny gramnegativní bakterie mají kompletní O-specifický polysacharidový řetězec sestávající z opakujících se oligosacharidových jednotek. Zejména bakterie rodu Neisseria mají krátký glykolipid nazývaný lipooligosacharid (LOS). Je srovnatelná s R formou, která ztratila specificitu O-antigenu, pozorovanou u mutantních drsných kmenů E-coli. Struktura VOC připomíná strukturu glykosfingolipidu lidské cytoplazmatické membrány, takže VOC napodobuje mikroba, což mu umožňuje vyhnout se imunitní reakci hostitele.
Matricové proteiny vnější membrány ji prostupují takovým způsobem, že proteinové molekuly tzv porinami, hraniční hydrofilní póry, kterými prochází voda a malé hydrofilní molekuly s relativní hmotností do 700 D.
Mezi vnější a cytoplazmatickou membránou je periplazmatický prostor, nebo periplazma obsahující enzymy (proteázy, lipázy, fosfatázy, nukleázy, β-laktamázy), stejně jako složky transportních systémů.
Když je syntéza bakteriální buněčné stěny narušena vlivem lysozymu, penicilinu, ochranných faktorů těla a dalších sloučenin, vznikají buňky se změněným (často kulovitým) tvarem: protoplasty- bakterie zcela postrádající buněčnou stěnu; sféroplasty- bakterie s částečně zachovanou buněčnou stěnou. Po odstranění inhibitoru buněčné stěny mohou takto změněné bakterie reverzovat, tzn. získat plnohodnotnou buněčnou stěnu a obnovit její původní tvar.
Bakterie typu sféroidů nebo protoplastů, které vlivem antibiotik nebo jiných faktorů ztratily schopnost syntetizovat peptidoglykan a jsou schopny se množit, jsou tzv. L-tvary(od názvu Institutu D. Listera, kde nejprve
byly studovány). L-formy mohou také vznikat v důsledku mutací. Jsou to osmoticky citlivé, kulovité, baňkovité buňky různých velikostí, včetně těch, které procházejí bakteriálními filtry. Některé L-formy (nestabilní), když je odstraněn faktor, který vedl ke změnám v bakteriích, se mohou obrátit a vrátit se k původní bakteriální buňce. L-formy mohou být produkovány mnoha patogeny infekčních chorob.
Cytoplazmatická membrána v elektronové mikroskopii ultratenkých řezů je to třívrstvá membrána (2 tmavé vrstvy, každá o tloušťce 2,5 nm, oddělené světlou mezilehlou). Strukturou je podobná plazmalemě živočišných buněk a skládá se z dvojité vrstvy lipidů, hlavně fosfolipidů, se zapuštěnými povrchovými a integrálními proteiny, které jakoby pronikají strukturou membrány. Některé z nich jsou permeázy podílející se na transportu látek. Na rozdíl od eukaryotických buněk cytoplazmatická membrána bakteriální buňky postrádá steroly (s výjimkou mykoplazmat).
Cytoplazmatická membrána je dynamická struktura s mobilními složkami, takže je považována za pohyblivou tekutou strukturu. Obklopuje vnější část cytoplazmy bakterií a podílí se na regulaci osmotického tlaku, transportu látek a energetickém metabolismu buňky (vlivem enzymů elektronového transportního řetězce, adenosintrifosfatázy – ATPázy aj.). Při nadměrném růstu (ve srovnání s růstem buněčné stěny) tvoří cytoplazmatická membrána invagináty - invaginace v podobě složitě pokroucených membránových struktur, tzv. mesozomy. Méně složitě stočené struktury se nazývají intracytoplazmatické membrány. Úloha mezozomů a intracytoplazmatických membrán není plně objasněna. Dokonce se předpokládá, že jde o artefakt, ke kterému dochází po přípravě (fixaci) vzorku pro elektronovou mikroskopii. Přesto se má za to, že deriváty cytoplazmatické membrány se účastní buněčného dělení, poskytují energii pro syntézu buněčné stěny a podílejí se na sekreci látek, sporulaci, tzn. v procesech s vysokou spotřebou energie. Cytoplazma zaujímá hlavní objem bakterií
buňka a skládá se z rozpustných proteinů, ribonukleových kyselin, inkluzí a četných malých granulí – ribozomů, odpovědných za syntézu (translaci) proteinů.
Ribozomy bakterie mají velikost asi 20 nm a sedimentační koeficient 70S, na rozdíl od 80S ribozomů charakteristických pro eukaryotické buňky. Některá antibiotika proto vazbou na bakteriální ribozomy inhibují syntézu bakteriálních proteinů bez ovlivnění syntézy proteinů v eukaryotických buňkách. Bakteriální ribozomy se mohou disociovat do dvou podjednotek: 50S a 30S. rRNA je konzervovaný prvek bakterií („molekulární hodiny“ evoluce). 16S rRNA je součástí malé ribozomální podjednotky a 23S rRNA je součástí velké ribozomální podjednotky. Studium 16S rRNA je základem genové systematiky, která umožňuje posoudit stupeň příbuznosti organismů.
Cytoplazma obsahuje různé inkluze ve formě glykogenových granulí, polysacharidů, kyseliny β-hydroxymáselné a polyfosfátů (volutin). Hromadí se při nadbytku živin v prostředí a působí jako rezervní látky pro potřeby výživy a energie.
Voljutin má afinitu k bazickým barvivům a je snadno detekován pomocí speciálních barvících metod (např. podle Neissera) ve formě metachromatických granulí. Toluidinovou modří nebo methylenovou modří se volutin zbarví červenofialově a cytoplazma bakterie se zbarví modře. Charakteristické uspořádání volutinových granulí je odhaleno u difterického bacilu ve formě intenzivně zbarvených buněčných pólů. Metachromatické zbarvení volutinu je spojeno s vysokým obsahem polymerovaného anorganického polyfosfátu. Pod elektronovou mikroskopií vypadají jako elektronově husté granule o velikosti 0,1-1 mikronu.
Nukleoid- ekvivalentní jádru u bakterií. Nachází se v centrální zóně bakterií ve formě dvouvláknové DNA, těsně sbalené jako koule. Nukleoid bakterií na rozdíl od eukaryot nemá jaderný obal, jadérko a bazické proteiny (histony). Většina bakterií obsahuje jeden chromozom, reprezentovaný molekulou DNA uzavřenou do kruhu. Ale některé bakterie mají dva prstencové chromozomy (V. cholerae) a lineární chromozomy (viz bod 5.1.1). Nukleoid je odhalen ve světelném mikroskopu po obarvení DNA-specifickými barvivy
metody: podle Feulgena nebo podle Romanovského-Giemsy. V elektronových difraktogramech ultratenkých sekcí bakterií se nukleoid jeví jako světelné zóny s fibrilárními vláknitými strukturami DNA vázanými v určitých oblastech k cytoplazmatické membráně nebo mezozomu zapojenému do replikace chromozomů.
Bakteriální buňka obsahuje kromě nukleoidu faktory extrachromozomální dědičnosti – plazmidy (viz část 5.1.2), což jsou kovalentně uzavřené kruhy DNA.
Kapsle, mikrokapsle, hlen.Kapsle - slizniční struktura o tloušťce více než 0,2 mikronu, pevně spojená s bakteriální buněčnou stěnou a mající jasně definované vnější hranice. Pouzdro je viditelné v otiskových stěrech z patologického materiálu. V čistých bakteriálních kulturách se pouzdro tvoří méně často. Detekuje se pomocí speciálních metod barvení stěru podle Burri-Ginse, který vytváří negativní kontrast látek kapsle: inkoust vytváří kolem kapsle tmavé pozadí. Pouzdro se skládá z polysacharidů (exopolysacharidů), někdy z polypeptidů, např. u bacilu antraxu se skládá z polymerů kyseliny D-glutamové. Kapsle je hydrofilní a obsahuje velké množství vody. Zabraňuje fagocytóze bakterií. Pouzdro je antigenní: protilátky proti pouzdru způsobují jeho zvětšení (reakce bobtnání pouzdra).
Tvoří se mnoho bakterií mikrokapsle- tvorba sliznice o tloušťce menší než 0,2 mikronu, detekovatelná pouze elektronovou mikroskopií.
Mělo by být odlišeno od kapsle sliz - mukoidní exopolysacharidy, které nemají jasné vnější hranice. Hlen je rozpustný ve vodě.
Mukoidní exopolysacharidy jsou charakteristické pro mukoidní kmeny Pseudomonas aeruginosa, které se často nacházejí ve sputu pacientů s cystickou fibrózou. Bakteriální exopolysacharidy se účastní adheze (přilnutí k substrátům); nazývají se také glykokalyx.
Pouzdro a sliz chrání bakterie před poškozením a vysycháním, protože jsou hydrofilní, dobře váží vodu a zabraňují působení ochranných faktorů makroorganismu a bakteriofágů.
Flagella bakterie určují pohyblivost bakteriální buňky. Bičíky jsou tenká vlákna, která na sebe berou
Pocházejí z cytoplazmatické membrány a jsou delší než samotná buňka. Tloušťka bičíků je 12-20 nm, délka 3-15 µm. Skládají se ze tří částí: spirálovitého vlákna, háčku a základního tělíska obsahujícího tyčinku se speciálními disky (jeden pár disků u grampozitivních bakterií a dva páry u gramnegativních bakterií). Bičíky jsou připojeny k cytoplazmatické membráně a buněčné stěně disky. Vzniká tak efekt elektromotoru s tyčí – rotorem – rotujícím bičíkem. Jako zdroj energie se využívá rozdíl protonového potenciálu na cytoplazmatické membráně. Rotační mechanismus zajišťuje protonová ATP syntetáza. Rychlost rotace bičíku může dosáhnout 100 ot./s. Pokud má bakterie několik bičíků, začnou se synchronně otáčet, proplétají se do jednoho svazku a tvoří jakousi vrtuli.
Bičíky jsou vyrobeny z bílkoviny zvané flagellin. (bičík- bičík), což je antigen - tzv. H-antigen. Bičíkové podjednotky jsou stočeny ve formě šroubovice.
Počet bičíků u různých druhů bakterií kolísá od jednoho (monotrichus) u Vibrio cholerae po desítky a stovky rozprostírajících se po obvodu bakterie (peritrichus), u Escherichia coli, Proteus atd. Lophotrichové mají na jednom konci svazek bičíků buňky. Amphitrichy má jeden bičík nebo svazek bičíků na opačných koncích buňky.
Bičíky se detekují pomocí elektronové mikroskopie přípravků potažených těžkými kovy, nebo ve světelném mikroskopu po úpravě speciálními metodami založenými na leptání a adsorpci různých látek vedoucí ke zvětšení tloušťky bičíků (např. po stříbření).
Villi nebo pili (fimbrie)- nitkovité útvary, tenčí a kratší (3-10 nm * 0,3-10 µm) než bičíky. Pili vybíhají z buněčného povrchu a jsou složeny z proteinu pilin. Je známo několik typů pili. Pili obecného typu jsou zodpovědné za připojení k substrátu, výživu a metabolismus voda-sůl. Jsou četné - několik stovek na buňku. Sex pili (1-3 na buňku) vytvářejí kontakt mezi buňkami a přenášejí mezi nimi genetickou informaci konjugací (viz kapitola 5). Zvláště zajímavé jsou pili typu IV, u kterých jsou konce hydrofobní, v důsledku čehož se tyto pili také nazývají kadeře; Umístění
Jsou umístěny na pólech buňky. Tyto pili se nacházejí v patogenních bakteriích. Mají antigenní vlastnosti, přivádějí bakterie do kontaktu s hostitelskou buňkou a podílejí se na tvorbě biofilmu (viz kapitola 3). Mnoho pili jsou receptory pro bakteriofágy.
Spory - zvláštní forma klidových bakterií s grampozitivním typem struktury buněčné stěny. Sporotvorné bakterie rodu Bacil, u nichž velikost spor nepřesahuje průměr buňky se nazývají bacily. Bakterie tvořící spory, u nichž velikost spory přesahuje průměr buňky, což způsobuje, že mají tvar vřetena, se nazývají klostridie, například bakterie rodu Clostridium(z lat. Clostridium- vřeteno). Spory jsou odolné vůči kyselinám, proto se barví červeně metodou Aujeszky nebo metodou Ziehl-Neelsen a vegetativní buňka se barví modře.
Sporulace, tvar a umístění spor v buňce (vegetativní) jsou druhovou vlastností bakterií, která umožňuje jejich vzájemné odlišení. Tvar výtrusů může být oválný nebo kulovitý, umístění v buňce je terminální, tzn. na konci tyčinky (u původce tetanu), subterminální - blíže ke konci tyčinky (u původců botulismu, plynové gangrény) a centrální (u bacilu antraxu).
Proces sporulace (sporulace) prochází řadou fází, při kterých dochází k oddělení části cytoplazmy a chromozomu bakteriální vegetativní buňky, obklopené prorůstající cytoplazmatickou membránou - vzniká prospora.
Protoplast prospory obsahuje nukleoid, systém syntetizující protein a systém produkce energie založený na glykolýze. Cytochromy chybí i v aerobech. Neobsahuje ATP, energie pro klíčení je uložena ve formě 3-glycerolfosfátu.
Prospora je obklopena dvěma cytoplazmatickými membránami. Vrstva obklopující vnitřní membránu výtrusy se nazývá stěna spor, skládá se z peptidoglykanu a je hlavním zdrojem buněčné stěny při klíčení spor.
Mezi vnější membránou a stěnou spor se vytvoří silná vrstva skládající se z peptidoglykanu, který má mnoho příčných vazeb - kůra.
Nachází se mimo vnější cytoplazmatickou membránu výtrusná skořápka, skládající se z proteinů podobných keratinu,
drží více intramolekulárních disulfidových vazeb. Tato skořepina poskytuje odolnost vůči chemickým činidlům. Spory některých bakterií mají další obal - exosporium lipoproteinové povahy. Tímto způsobem se vytvoří vícevrstvá, špatně propustná skořepina.
Sporulace je doprovázena intenzivní konzumací prosporou a následně vyvíjejícím se obalem spor kyseliny dipikolinové a iontů vápníku. Spóra získává tepelnou odolnost, která je spojena s přítomností dipikolinátu vápenatého v ní.
Spóra může přetrvávat po dlouhou dobu kvůli přítomnosti vícevrstvé skořápky, dipikolinátu vápenatého, nízkému obsahu vody a pomalým metabolickým procesům. Například v půdě mohou patogeny antraxu a tetanu přetrvávat desítky let.
Za příznivých podmínek spory klíčí a procházejí třemi po sobě jdoucími fázemi: aktivace, iniciace, růst. V tomto případě se z jedné spory vytvoří jedna bakterie. Aktivace je připravenost ke klíčení. Při teplotě 60-80 °C se spóra aktivuje ke klíčení. Iniciace klíčení trvá několik minut. Fáze rozrůstání se vyznačuje rychlým růstem, doprovázeným destrukcí skořápky a rašením semenáčku.
2.2.3. Strukturní rysy spirochet, rickettsie, chlamydií, aktinomycet a mykoplazmat
Spirochety- tenké dlouhé spletité bakterie. Skládají se z vnější membránové buněčné stěny, která obklopuje cytoplazmatický válec. Na vršku vnější membrány je průhledný kryt glykosaminoglykanové povahy. Pod vnější membránou buněčné stěny jsou fibrily, které se stáčejí kolem cytoplazmatického válce a dávají bakteriím šroubovitý tvar. Fibrily jsou připojeny ke koncům buňky a směřují k sobě. Počet a uspořádání fibril se u jednotlivých druhů liší. Fibrily se podílejí na pohybu spirochet, dávají buňkám rotační, ohýbací a translační pohyb. V tomto případě spirochety tvoří smyčky, kadeře a ohyby, které se nazývají sekundární kadeře. Spirochety nevnímají dobře barviva. Obvykle jsou malované podle Romanovského-Giemsy nebo postříbřené. Žít
Forma spirochety se zkoumá pomocí mikroskopie s fázovým kontrastem nebo v tmavém poli.
Spirochety jsou zastoupeny třemi rody, které jsou pro člověka patogenní: Treponema, Borrelia, Leptospira.
Treponema(rod treponema) mají vzhled tenkých, vývrtkou kroucených nití s 8-12 jednotnými malými kadeřemi. Kolem protoplastu treponému jsou 3-4 fibrily (bičíky). Cytoplazma obsahuje cytoplazmatická vlákna. Patogenní zástupci jsou T. pallidum- původce syfilis, T. pertenue- původce tropické choroby yaws. Existují také saprofyti - obyvatelé lidské ústní dutiny a bahna nádrží.
Borrelie(rod Borrelie), na rozdíl od treponém jsou delší, mají 3-8 velkých kadeří a 7-20 fibril. Patří mezi ně původce recidivující horečky (B. recurrentis) a patogeny lymské boreliózy (V. burgdorferi) a další nemoci.
Leptospira(rod Leptospira) Mají mělké a časté kadeře ve formě zkrouceného lana. Konce těchto spirochet jsou zakřivené jako háčky se zesílením na koncích. Tvoří sekundární kadeře a mají tvar písmen S nebo C; mají dvě axiální fibrily. Patogenní zástupce L. interrogans způsobuje leptospirózu při požití vodou nebo jídlem, což vede ke krvácení a žloutence.
Rickettsie mají metabolismus nezávislý na hostitelské buňce, je však možné, že ke své reprodukci přijímají vysokoenergetické sloučeniny z hostitelské buňky. V nátěrech a tkáních jsou obarveny podle Romanovského-Giemsy, podle Macchiavella-Zdrodovského (rickettsie jsou červené a infikované buňky modré).
U lidí způsobují rickettsie epidemický tyfus. (R. prowazekii), rickettsióza přenášená klíšťaty (R. sibirica), Rocky Mountain skvrnitá horečka (R. rickettsii) a další rickettsiózy.
Struktura jejich buněčné stěny se podobá struktuře gramnegativních bakterií, i když existují rozdíly. Neobsahuje typický peptidoglykan: zcela postrádá kyselinu N-acetylmuramovou. Buněčná stěna se skládá z dvojité vnější membrány, která obsahuje lipopolysacharid a proteiny. I přes nepřítomnost peptidoglykanu je buněčná stěna chlamydií tuhá. Cytoplazma buňky je omezena vnitřní cytoplazmatickou membránou.
Hlavní metodou pro detekci chlamydií je barvení podle Romanovského-Giemsy. Barva závisí na fázi životního cyklu: elementární tělíska vypadají fialově na pozadí modré cytoplazmy buňky, retikulární tělíska vypadají modře.
U člověka způsobují chlamydie poškození očí (trachom, konjunktivitida), urogenitálního traktu, plic atd.
Actinomycetes- větvené, vláknité nebo tyčinkovité grampozitivní bakterie. Jeho jméno (z řečtiny. actis- Rayi, mykes- plísně), které dostaly v důsledku tvorby drúz v postižených tkáních - granule pevně propletených vláken ve formě
paprsky vybíhající ze středu a končící baňkovitým ztluštěním. Aktinomycety tvoří podobně jako houby mycelium – nitkovité propletené buňky (hyfy). Tvoří substrátové mycelium, které vzniká vrůstáním buněk do živného média, a vzdušné mycelium, které roste na povrchu média. Aktinomycety se mohou dělit fragmentací mycelia na buňky podobné tyčinkovitým a kokoidním bakteriím. Na vzdušných hyfách aktinomycet se tvoří spory, které slouží k rozmnožování. Výtrusy aktinomycet obvykle nejsou odolné vůči teplu.
Společnou fylogenetickou větev s aktinomycetami tvoří tzv. nokardiformní (nokardioformní) aktinomycety - kolektivní skupina tyčinkovitých bakterií nepravidelného tvaru. Jejich jednotliví zástupci tvoří větvené formy. Patří mezi ně bakterie rodů Corynebacterium, Mycobacterium, Nocardia atd. Aktinomycety podobné Nocardi se vyznačují přítomností cukrů arabinózy, galaktózy, jakož i mykolových kyselin a velkého množství mastných kyselin v buněčné stěně. Kyseliny mykolové a lipidy buněčné stěny určují odolnost bakterií vůči kyselinám, zejména mykobakterií tuberkulóza a lepra (při barvení podle Ziehla-Neelsena jsou červené, bakterie a tkáňové prvky nerezistentní vůči kyselinám, sputum jsou modré).
Patogenní aktinomycety způsobují aktinomykózu, nokardie - nokardióza, mykobakterie - tuberkulóza a lepra, korynebakterie - záškrt. V půdě jsou rozšířeny saprofytické formy aktinomycet a nokardiformní aktinomycety, mnohé z nich jsou producenty antibiotik.
Mykoplazmata- malé bakterie (0,15-1 µm), obklopené pouze cytoplazmatickou membránou obsahující steroly. Patří do třídy Mollicutes. Vzhledem k absenci buněčné stěny jsou mykoplazmata osmoticky citlivá. Mají různé tvary: kokoidní, vláknité, baňkovité. Tyto formy jsou viditelné pod mikroskopem s fázovým kontrastem čistých kultur mykoplazmat. Na hustém živném médiu tvoří mykoplazmata kolonie, které připomínají smažená vejce: centrální neprůhledná část ponořená do média a průsvitný okraj ve formě kruhu.
Mykoplazmata způsobují u lidí atypický zápal plic (Mycoplasma pneumoniae) a léze genitourinárního traktu
(M. hominis atd.). Mykoplazmata způsobují onemocnění nejen zvířat, ale i rostlin. Dost rozšířeni jsou i nepatogenní zástupci.
2.3. Struktura a klasifikace hub
Houby patří do domény eukarya, království Houby (Mycota, Mycetes). V poslední době jsou houby a prvoci rozděleni do samostatných říší: království Eumycota(pravé houby), království Chromista a království Prvoci. Některé mikroorganismy dříve považované za houby nebo prvoky byly přesunuty do nové říše Chromista(chromové desky). Houby jsou mnohobuněčné nebo jednobuněčné nefotosyntetické (bez chlorofylu) eukaryotické mikroorganismy se silnou buněčnou stěnou. Mají jádro s jaderným obalem, cytoplazmu s organelami, cytoplazmatickou membránu a vícevrstvou tuhou buněčnou stěnu složenou z několika typů polysacharidů (mannany, glukany, celulóza, chitin), dále bílkovin, lipidů atd. Některé houby tvoří tzv. kapsle. Cytoplazmatická membrána obsahuje glykoproteiny, fosfolipidy a ergosteroly (na rozdíl od cholesterolu, hlavního sterolu savčích tkání). Většina hub jsou povinné nebo fakultativní aeroby.
Houby jsou v přírodě rozšířené, zejména v půdě. Některé houby přispívají k výrobě chleba, sýrů, produktů kyseliny mléčné a alkoholu. Jiné houby produkují antimikrobiální antibiotika (např. penicilin) a imunosupresiva (např. cyklosporin). Houby používají genetici a molekulární biologové k modelování různých procesů. Fytopatogenní houby způsobují značné škody v zemědělství, způsobují houbové choroby obilnin a obilí. Infekce způsobené houbami se nazývají mykózy. Existují hyfové a kvasinkové houby.
Hyfové (plísňové) houby nebo hyphomycetes se skládají z tenkých vláken o tloušťce 2-50 mikronů, nazývaných hyfy, které jsou vetkány do mycelia nebo mycelia (plísně). Tělo houby se nazývá stélka. Existují hyfomycety demacium (pigmentované - hnědé nebo černé) a hyalinní (nepigmentované). Hyfy, které prorůstají do živného substrátu, jsou zodpovědné za výživu houby a nazývají se vegetativní hyfy. Hyphae, ra-
stojící nad povrchem substrátu se nazývají vzdušné nebo reprodukční hyfy (zodpovědné za reprodukci). Kolonie mají načechraný vzhled díky vzdušnému myceliu.
Existují nižší a vyšší houby: hyfy vyšších hub jsou odděleny přepážkami nebo přepážkami s otvory. Hyfy nižších hub nemají přepážky, jsou to mnohojaderné buňky zvané koenocytární (z řečtiny. koenos- jediný, společný).
Kvasinkové houby (kvasinky) jsou zastoupeny především jednotlivými oválnými buňkami o průměru 3-15 mikronů a jejich kolonie mají na rozdíl od hyfových hub kompaktní vzhled. Podle typu pohlavního rozmnožování jsou rozděleny mezi vyšší houby - askomycety a bazidiomycety. Při nepohlavním rozmnožování kvasinky pučí nebo se dělí. Mohou tvořit pseudohyfy a falešné mycelium (pseudomycelium) ve formě řetězců protáhlých buněk - „klobásů“. Houby, které jsou podobné kvasinkám, ale nemají sexuální způsob rozmnožování, se nazývají kvasinky. Rozmnožují se pouze nepohlavně – pučením nebo štěpením. Pojmy „houby podobné kvasinkám“ jsou často ztotožňovány s pojmem „kvasinky“.
Mnoho hub má dimorfismus - schopnost růst hyfální (myceliální) nebo kvasinkovitý, v závislosti na kultivačních podmínkách. V infikovaném organismu rostou ve formě kvasinkovitých buněk (kvasinková fáze) a na živných půdách tvoří hyfy a mycelium. Dimorfismus je spojen s teplotním faktorem: při pokojové teplotě se tvoří mycelium a při 37 ° C (při teplotě lidského těla) se tvoří buňky podobné kvasinkám.
Houby se rozmnožují pohlavně nebo nepohlavně. K pohlavnímu rozmnožování hub dochází s tvorbou gamet, pohlavních spor a jiných sexuálních forem. Pohlavní formy se nazývají teleomorfové.
Nepohlavní rozmnožování hub nastává s tvorbou odpovídajících forem nazývaných anamorfy. K takové reprodukci dochází pučením, fragmentací hyf a nepohlavních spor. Endogenní výtrusy (sporangiospory) dozrávají uvnitř kulaté struktury – sporangia. Exogenní výtrusy (konidie) se tvoří na špičkách plodových hyf, tzv. konidiofory.
Existuje celá řada konidií. Arthrokonidie (artrospory), neboli tallokonidie, vznikají rovnoměrným septováním a rozkouskováním hyf a blastokonidie vznikají v důsledku pučení. Malé jednobuněčné konidie se nazývají mikrokonidie, velké mnohobuněčné konidie se nazývají makrokonidie. Mezi asexuální formy hub patří také chlamydokondie neboli chlamydospory (silnostěnné velké klidové buňky nebo komplex malých buněk).
Existují dokonalé a nedokonalé houby. Dokonalé houby mají sexuální způsob rozmnožování; mezi ně patří zygomycety (Zygomycota), ascomycetes (Ascomycota) a bazidiomycety (Basidiomycota). Nedokonalé houby mají pouze nepohlavní rozmnožování; Patří mezi ně formální konvenční typ/skupina hub – deuteromycety (Deiteromycota).
Zygomycety patří k nižším houbám (neseptické mycelium). Patří mezi ně zástupci rodů Mucor, Rhizopus, Rhizomucor, Absidia, Basidiobolus, Conidiobolus. Distribuováno v půdě a vzduchu. Mohou způsobit zygomykózu (mukoromykózu) plic, mozku a dalších lidských orgánů.
Při nepohlavním rozmnožování zygomycet se na plodné hyfě (sporangiofory) tvoří sporangium - kulovité ztluštění se schránkou obsahující četné sporangiospory (obr. 2.6, 2.7). K pohlavnímu rozmnožování u zygomycet dochází pomocí zygospor.
Ascomycetes (vačnatci) mají přepážkové mycelium (kromě jednobuněčných kvasinek). Svůj název dostaly podle hlavního plodného orgánu - bursa neboli ascus, obsahující 4 nebo 8 haploidních pohlavních spor (askospor).
Ascomycetes zahrnují jednotlivé zástupce (teleomorfy) rodů Aspergillus A Plísně Penicillium. Většina rodů hub Aspergillus, Penicillium jsou anamorfní, tzn. rozmnožují se jen bezmocně
 Rýže. 2.6. Houby rodu Mucor(obrázek A.S. Bykov)
Rýže. 2.6. Houby rodu Mucor(obrázek A.S. Bykov)
 Rýže. 2.7. Houby rodu Rhizopus. Vývoj sporangia, sporangiospor a rhizoidů
Rýže. 2.7. Houby rodu Rhizopus. Vývoj sporangia, sporangiospor a rhizoidů
přímo pomocí nepohlavních výtrusů - konidií (obr. 2.8, 2.9) a je třeba je podle této charakteristiky zařadit mezi nedokonalé houby. V houbách rod Aspergillus na koncích plodových hyf, konidioforů, jsou ztluštění - sterigmata, fialidy, na kterých se tvoří řetízky konidií („vodní plíseň“).
V houbách rod plísně Penicillium(střapec) plodová hyfa se podobá štětce, neboť se z ní (na konidioforu) tvoří ztluštěniny rozvětvující se do menších struktur - sterigmata, fialidy, na kterých jsou řetízky konidií. Některé druhy Aspergillus mohou způsobit aspergilózu a aflatoxikózu a Penicillium může způsobit peniciliózu.
Zástupci askomycet jsou teleomorfy rodů Trichophyton, Microsporum, Histoplasma, Blastomyces, stejně jako otřesy
 Rýže. 2.8. Houby rodu Plísně Penicillium.Řetězce konidií se táhnou od fialid
Rýže. 2.8. Houby rodu Plísně Penicillium.Řetězce konidií se táhnou od fialid
 Rýže. 2.9. Houby rodu Aspergillus fumigatus.Řetězce konidií se táhnou od fialid
Rýže. 2.9. Houby rodu Aspergillus fumigatus.Řetězce konidií se táhnou od fialid
Mezi basidiomycety patří kloboukové houby. Mají přepážkové mycelium a vytvářejí pohlavní spory - basidiospory odtržením od bazidia - terminální buňky mycelia, homologní s ascus. Mezi basidiomycety patří některé kvasinky, jako jsou teleomorfy Cryptococcus neoformans.
Deuteromycety jsou nedokonalé houby (Fungi imperfecti, anamorfní houby, konidiové houby). Jedná se o podmíněný, formální taxon hub, spojující houby, které nemají pohlavní rozmnožování. Nedávno byl místo termínu „deuteromycetes“ navržen termín „mitosporózní houby“ – houby, které se rozmnožují nepohlavními sporami, tzn. mitózou. Když je zjištěna skutečnost pohlavního rozmnožování nedokonalých hub, jsou převedeny na jeden ze známých typů - Ascomycota nebo Basidiomycota přiřazení jména k teleomorfní formě. Deuteromycety mají přepážkové mycelium a rozmnožují se pouze nepohlavní tvorbou konidií. Mezi deuteromycety patří nedokonalé kvasinky (houby podobné kvasinkám), například některé houby rodu Candida, postihující kůži, sliznice a vnitřní orgány (kandidóza). Jsou oválného tvaru, 2-5 mikronů v průměru, dělí se pučením, tvoří pseudohyfy (pseudomycelium) ve formě řetězců protáhlých buněk a někdy tvoří hyfy. Pro Candida albicans charakteristická je tvorba chlamydospor (obr. 2.10). Mezi deuteromycety patří také další houby, které nemají pohlavní způsob rozmnožování, patřící do rodů Epidermophyton, Coccidioides, Paracoccidioides, Sporothrix, Aspergillus, Phialophora, Fonsecaea, Exophiala, Cladophialophora, Bipolaris, Exerohilum, Wangiella, Alrernaria atd.
 Rýže. 2.10. Houby rodu Candida albicans(obrázek A.S. Bykov)
Rýže. 2.10. Houby rodu Candida albicans(obrázek A.S. Bykov)
2.4. Struktura a klasifikace prvoků
Nejjednodušší patří do domény eukarya, zvířecí království (zvířata), podříše Prvoci. Nedávno bylo navrženo zařadit prvoky do hodnosti království Prvoci.
Protozoální buňka je obklopena membránou (pelikulou) - obdobou cytoplazmatické membrány živočišných buněk. Má jádro s jaderným obalem a jadérkem, cytoplazmu obsahující endoplazmatické retikulum, mitochondrie, lysozomy a ribozomy. Velikost prvoků se pohybuje od 2 do 100 mikronů. Při barvení podle Romanovského-Giemsy je jádro prvoka červené a cytoplazma modrá. Prvoci se pohybují pomocí bičíků, řasinek nebo pseudopodií, někteří z nich mají trávicí a kontraktilní (vylučovací) vakuoly. Mohou se živit v důsledku fagocytózy nebo tvorby speciálních struktur. Podle typu výživy se dělí na heterotrofní a autotrofní. Mnoho prvoků (dysenterická améba, Giardia, Trichomonas, Leishmania, Balantidia) může růst na živných půdách obsahujících nativní proteiny a aminokyseliny. K jejich kultivaci se využívají i buněčné kultury, kuřecí embrya a laboratorní zvířata.
Prvoci se rozmnožují nepohlavně – dvojitým nebo vícenásobným (schizogonie) dělením, někteří i pohlavně (sporogonie). Někteří prvoci se rozmnožují extracelulárně (Giardia), jiní se rozmnožují intracelulárně (Plasmodium, Toxoplasma, Leishmania). Životní cyklus prvoků je charakterizován stádii - vznik stádia trofozoitu a stádia cysty. Cysty jsou klidová stádia, odolná vůči změnám teploty a vlhkosti. Cysty jsou odolné vůči kyselinám Sarcocystis, Cryptosporidium A Isospora.
Dříve byli prvoci způsobující onemocnění u lidí zastoupeni 4 typy 1 ( Sarcomastigophora, Apicomplexa, Ciliophora, Microspora). Tyto typy byly nedávno překlasifikovány do většího počtu a objevila se nová království – Prvoci A Chromista(Tabulka 2.2). Do nového království Chromista(chromovici) zahrnovali některé prvoky a houby (blastocysty, oomycety a Rhinosporidium seeberi). Království Prvoci zahrnuje améby, bičíkovce, sporozoány a nálevníky. Dělí se na různé typy, mezi které patří améby, bičíkovci, sporozoáni a nálevníci.
Tabulka 2.2. Zástupci království Prvoci A Chromista, lékařského významu
 1 Typ Sarcomastigophora sestával z podtypů Sarcodina A Mastigophora. Podtyp Sarcodina(sarcodaceae) zahrnovaly dysenterickou amébu a podtyp Mastigophora(bičíkovci) - trypanozomy, leishmanie, lamblie a trichomonas. Typ Apicomplexa zahrnutá třída Sporozoa(spory), které zahrnovaly plasmodia malárie, toxoplazma, kryptosporidium atd. Typ Ciliophora zahrnuje balantidia a typ Microspora- mikrosporidie.
1 Typ Sarcomastigophora sestával z podtypů Sarcodina A Mastigophora. Podtyp Sarcodina(sarcodaceae) zahrnovaly dysenterickou amébu a podtyp Mastigophora(bičíkovci) - trypanozomy, leishmanie, lamblie a trichomonas. Typ Apicomplexa zahrnutá třída Sporozoa(spory), které zahrnovaly plasmodia malárie, toxoplazma, kryptosporidium atd. Typ Ciliophora zahrnuje balantidia a typ Microspora- mikrosporidie.
Konec stolu. 2.2
 Mezi améby patří původce lidské amébózy – amébová úplavice (Entamoeba histolytica), volně žijící a nepatogenní améby (améby střevní aj.). Améby se binárně rozmnožují nepohlavně. Jejich životní cyklus se skládá ze stádia trofozoitu (rostoucí, pohyblivá buňka, slabě stabilní) a stádia cysty. Trophozoiti se pohybují pomocí pseudopodií, které zachycují a ponořují živiny do cytoplazmy. Z
Mezi améby patří původce lidské amébózy – amébová úplavice (Entamoeba histolytica), volně žijící a nepatogenní améby (améby střevní aj.). Améby se binárně rozmnožují nepohlavně. Jejich životní cyklus se skládá ze stádia trofozoitu (rostoucí, pohyblivá buňka, slabě stabilní) a stádia cysty. Trophozoiti se pohybují pomocí pseudopodií, které zachycují a ponořují živiny do cytoplazmy. Z
Trofozoit tvoří cystu, která je odolná vůči vnějším faktorům. Jakmile se dostane do střeva, změní se na trofozoit.
Bičíkovci se vyznačují přítomností bičíků: Leishmania má jeden bičík, Trichomonas má 4 volné bičíky a jeden bičík spojený s krátkou zvlněnou membránou. Oni jsou:
Bičíkovci krve a tkání (Leishmania - původci leishmaniózy; Trypanozomy - původci spavé nemoci a Chagasovy choroby);
Střevní bičíkovci (giardia - původce giardiózy);
Bičíkovci urogenitálního traktu (Trichomonas vaginalis - původce trichomoniázy).
Ty řasnaté jsou zastoupeny balantidiemi, které postihují lidské tlusté střevo (balantidiasis dyzentery). Balantidia mají stádium trofozoitu a cysty. Trofozoit je pohyblivý, má četné řasinky, tenčí a kratší než bičíky.
2.5. Struktura a klasifikace virů
Viry jsou nejmenší mikroby patřící do království Virae(z lat. virus- já). Nemají buněčnou strukturu a skládají se
Struktura virů, vzhledem k jejich malé velikosti, je studována pomocí elektronové mikroskopie jak virionů, tak jejich ultratenkých řezů. Velikosti virů (virionů) se určují přímo pomocí elektronové mikroskopie nebo nepřímo ultrafiltrací přes filtry se známým průměrem pórů, případně ultracentrifugací. Velikost virů se pohybuje od 15 do 400 nm (1 nm se rovná 1/1000 µm): malé viry, jejichž velikost je podobná velikosti ribozomů, zahrnují parvoviry a polioviry a největší viry variola (350 nm). Viry se liší tvarem svých virionů, které mají podobu tyčinek (virus tabákové mozaiky), kuliček (virus vztekliny), kuliček (viry poliomyelitidy, HIV), vláken (filoviry), spermií (mnoho bakteriofágů).
Viry ohromují představivost svou rozmanitostí struktury a vlastností. Na rozdíl od buněčných genomů, které obsahují jednotnou dvouvláknovou DNA, jsou virové genomy extrémně rozmanité. Existují DNA a RNA viry, které jsou haploidní, tzn. mají jednu sadu genů. Diploidní genom mají pouze retroviry. Genom virů obsahuje od 6 do 200 genů a je reprezentován různými typy nukleových kyselin: dvouvláknovými, jednovláknovými, lineárními, kruhovými, fragmentovanými.
Mezi jednořetězcovými RNA viry se rozlišuje genomová plus-řetězcová RNA a minus-řetězcová RNA (polarita RNA). Kladné vlákno (pozitivní vlákno) RNA těchto virů, kromě genomické (dědičné) funkce, plní funkci informační nebo messengerové RNA (mRNA nebo mRNA); je to matrice pro syntézu proteinů na ribozomech infikované buňky. Plus-vláknová RNA je infekční: když je zavedena do citlivých buněk, může způsobit infekční proces.
cess. Mínusové vlákno (negativní vlákno) RNA virů plní pouze dědičnou funkci; Pro syntézu proteinů se na záporném vláknu RNA syntetizuje komplementární řetězec. Některé viry mají ambipolární RNA genom (ambisense z řečtiny ambi- na obou stranách dvojitá komplementarita), tzn. obsahuje plus a mínus segmenty RNA.
Existují jednoduché viry (například virus hepatitidy A) a komplexní viry (například viry chřipky, herpes, koronaviry).
Jednoduché nebo neobalené viry mají pouze nukleovou kyselinu spojenou s proteinovou strukturou zvanou kapsida (z lat. capsa- pouzdro). Proteiny spojené s nukleovou kyselinou jsou známé jako nukleoproteiny a spojení virových kapsidových proteinů s virovou nukleovou kyselinou se nazývá nukleokapsida. Některé jednoduché viry mohou tvořit krystaly (např. virus slintavky a kulhavky).
Kapsida obsahuje opakující se morfologické podjednotky - kapsomery, složené z několika polypeptidů. Nukleová kyselina virionu se váže na kapsidu za vzniku nukleokapsidy. Kapsida chrání nukleovou kyselinu před degradací. U jednoduchých virů se kapsida podílí na připojení (adsorpci) k hostitelské buňce. Jednoduché viry opouštějí buňku v důsledku její destrukce (lýzy).
Komplexní neboli obalené viry (obr. 2.11) mají kromě kapsidy membránový dvojitý lipoproteinový obal (synonymum: superkapsida nebo peplos), který se získává pučením virionu přes buněčnou membránu, např. plazmatická membrána, jaderná membrána nebo membrána endoplazmatického retikula. Virový obal obsahuje hroty glykoproteinu,
nebo trny, peplomery. Zničení skořápky éterem a jinými rozpouštědly inaktivuje složité viry. Pod skořápkou některých virů je matricový protein (M protein).
Viriony mají šroubovicovou, ikosaedrickou (kubickou) nebo komplexní typ kapsidové (nukleokapsid) symetrie. Helikální typ symetrie je způsoben helikální strukturou nukleokapsidy (například u chřipkových virů, koronavirů): kapsomery jsou uspořádány do spirály spolu s nukleovou kyselinou. Ikosahedrický typ symetrie je způsoben vytvořením izometricky dutého tělesa z kapsidy obsahující virovou nukleovou kyselinu (například u herpes viru).
Kapsida a obal (superkapsida) chrání viriony před vlivy prostředí a určují selektivní interakci (adsorpci) jejich receptorových proteinů s určitými
 Rýže. 2.11. Struktura obalených virů s ikosaedrickou (a) a šroubovicovou (b) kapsidou
Rýže. 2.11. Struktura obalených virů s ikosaedrickou (a) a šroubovicovou (b) kapsidou
oplodněné buňky, stejně jako antigenní a imunogenní vlastnosti virionů.
Vnitřní struktury virů se nazývají jádro. U adenovirů se jádro skládá z proteinů podobných histonům spojených s DNA, u reovirů - z proteinů vnitřní kapsidy.
Nositel Nobelovy ceny D. Baltimore navrhl baltimorský klasifikační systém založený na mechanismu syntézy mRNA. Tato klasifikace řadí viry do 7 skupin (tabulka 2.3). Mezinárodní výbor pro taxonomii virů (ICTV) přijal univerzální klasifikační systém, který používá taxonomické kategorie, jako je rodina (jméno končící na viridae), podrodina (jméno končí na virinae), rod (jméno končí na virus). Druh viru nedostal binomické jméno, jako bakterie. Viry jsou klasifikovány podle typu nukleové kyseliny (DNA nebo RNA), její struktury a počtu vláken. Mají dvouřetězcové nebo jednořetězcové nukleové kyseliny; pozitivní (+), negativní (-) polarita nukleové kyseliny nebo smíšená polarita nukleové kyseliny, ambipolární (+, -); lineární nebo kruhová nukleová kyselina; fragmentovaná nebo nefragmentovaná nukleová kyselina. Dále se bere velikost a morfologie virionů, počet kapsomer a typ symetrie nukleokapsidy, přítomnost obalu (superkapsidy), citlivost na éter a deoxycholát, místo rozmnožování v buňce, antigenní vlastnosti atd. v úvahu.
Tabulka 2.3. Hlavní viry lékařského významu
 Pokračování tabulky. 2.3
Pokračování tabulky. 2.3
 Konec stolu. 2.3
Konec stolu. 2.3
 Viry infikují zvířata, bakterie, houby a rostliny. Jako hlavní původci lidských infekčních onemocnění se viry podílejí také na procesech karcinogeneze a mohou být přenášeny různými způsoby, včetně placenty (virus zarděnek, cytomegalovirus atd.), které ovlivňují lidský plod. Mohou také vést k postinfekčním komplikacím - rozvoji myokarditidy, pankreatitidy, imunodeficience atd.
Viry infikují zvířata, bakterie, houby a rostliny. Jako hlavní původci lidských infekčních onemocnění se viry podílejí také na procesech karcinogeneze a mohou být přenášeny různými způsoby, včetně placenty (virus zarděnek, cytomegalovirus atd.), které ovlivňují lidský plod. Mohou také vést k postinfekčním komplikacím - rozvoji myokarditidy, pankreatitidy, imunodeficience atd.
Kromě virů zahrnují nebuněčné formy života priony a viroidy. Viroidy jsou malé molekuly kruhové, nadšroubovicové RNA, které neobsahují bílkoviny a způsobují onemocnění rostlin. Patologické priony jsou infekční proteinové částice, které způsobují zvláštní konformační onemocnění v důsledku změn ve struktuře normálního buněčného prionového proteinu ( PrP c), který je přítomen v těle zvířat a lidí. PrP s plní regulační funkce. Je kódován normálním prionovým genem (PrP genem), který se nachází na krátkém raménku lidského chromozomu 20. Prionová onemocnění se vyskytují jako přenosné spongiformní encefalopatie (Creutzfeldt-Jakobova choroba, kuru aj.). V tomto případě nabývá prionový protein jinou, infekční formu, označenou jako PrP sc(sc od scrapie- scrapie je prionová infekce ovcí a koz). Tento infekční prionový protein má vzhled fibril a od normálního prionového proteinu se liší svou terciární nebo kvartérní strukturou.
Úkoly pro sebepřípravu (sebeovládání)
A. Označte mikroby, které jsou prokaryota:
2. Viry.
3. Bakterie.
4. Priony.
B. Všimněte si charakteristických rysů prokaryotické buňky:
1. 70S ribozomy.
2. Přítomnost peptidoglykanu v buněčné stěně.
3. Přítomnost mitochondrií.
4. Diploidní soubor genů.
V. Označte složky peptidoglykanu:
1. Teichoové kyseliny.
2. N-acetylglukosamin.
3. Lipopolysarid.
4. Tetrapeptid.
G. Všimněte si strukturních rysů buněčné stěny gramnegativních bakterií:
1. Kyselina mesodiaminopimelová.
2. Teichoové kyseliny.
4. Porinové proteiny.
D. Vyjmenujte funkce spór u bakterií:
1. Zachování druhu.
2. Tepelná odolnost.
3. Rozptýlení substrátu.
4. Reprodukce.
1. Rickettsie.
2. Aktinomycety.
3. Spirochety.
4. Chlamydie.
A. Vyjmenujte vlastnosti aktinomycet:
1. Mají termolabilní výtrusy.
2. Grampozitivní bakterie.
3. Neexistuje žádná buněčná stěna.
4. Mají svinutý tvar.
Z. Vyjmenuj vlastnosti spirochet:
1. Gramnegativní bakterie.
2. Mají motorický fibrilární aparát.
3. Mají svinutý tvar.
A. Pojmenujte prvoky, kteří mají apikální komplex, který jim umožňuje proniknout do buňky:
1. Malarické plazmodium.
3. Toxoplasma.
4. Cryptosporidium.
NA. Pojmenujte charakteristický rys komplexních virů:
1. Dva typy nukleových kyselin.
2. Přítomnost lipidové membrány.
3. Dvojitá kapsida.
4. Přítomnost nestrukturních proteinů. L. Označte vyšší houby:
1. Mucor.
2. Candida.
3. Plísně Penicillium.
4. Aspergillus.
Bakteriální buňce chybí jádro, chromozomy jsou volně umístěny v cytoplazmě. Bakteriální buňce navíc chybí membránové organely: mitochondrie, EPS, Golgiho aparát atd. Vnější strana buněčné membrány je pokryta buněčnou stěnou.



Většina bakterií se pohybuje pasivně pomocí proudů vody nebo vzduchu. Pouze některé z nich mají organely pohybu - bičíky. Prokaryotické bičíky mají velmi jednoduchou strukturu a skládají se z proteinu bičíku, který tvoří dutý válec o průměru 10–20 nm. Šroubují se do média a pohánějí buňku dopředu. Zřejmě se jedná o jedinou známou stavbu v přírodě, která využívá princip kola.
Podle tvaru se bakterie dělí do několika skupin:
Koky (mají kulatý tvar);
- bacily (mají tyčinkovitý tvar);
- spirilla (mají tvar spirály);
- vibrios (ve tvaru čárky).
Podle způsobu dýchání se bakterie dělí na aerobní (většina bakterií) a anaeroby (původci tetanu, botulismu, plynatosti). Ti první potřebují k dýchání kyslík, pro ty druhé je kyslík zbytečný nebo dokonce jedovatý.

Struktura prokaryotické buňky. Prokaryotická buňka je mnohem jednodušší než živočišné a rostlinné buňky. Zvenčí je pokryta buněčnou stěnou, která plní ochranné, formativní a transportní funkce. Tuhost buněčné stěny zajišťuje murein. Někdy je bakteriální buňka nahoře pokryta kapslí nebo slizniční vrstvou.
Protoplazma bakterií je stejně jako u eukaryot obklopena plazmatickou membránou. Vakové, tubulární nebo lamelární invaginace membrány obsahují mezozomy zapojené do procesu dýchání, bakteriochlorofyl a další pigmenty.
Genetický materiál prokaryot netvoří jádro, ale nachází se přímo v cytoplazmě. Bakteriální DNA je jedna kruhová molekula, z nichž každá se skládá z tisíců a milionů nukleotidových párů. Genom bakteriální buňky je mnohem jednodušší než genom buněk vyvinutějších tvorů: v průměru obsahuje bakteriální DNA několik tisíc genů.
V prokaryotických buňkách není žádné endoplazmatické retikulum a ribozomy volně plují v cytoplazmě. Prokaryota nemají mitochondrie; Jejich funkce částečně plní buněčná membrána.
Mobilitu bakterií zajišťují bičíky. Bakterie se množí dělením přibližně každých 20 minut (za příznivých podmínek). DNA se replikuje, přičemž každá dceřiná buňka obdrží svou vlastní kopii rodičovské DNA. Je také možné přenášet DNA mezi nedělícími se buňkami (záchytem „nahé“ DNA, pomocí bakteriofágů nebo konjugací, kdy jsou bakterie navzájem spojeny kopulačními fimbriemi), ale počet jedinců se tím nezvyšuje. Reprodukci brání sluneční paprsky a produkty jejich vlastní životně důležité činnosti.
Chování bakterií není nijak zvlášť složité. Chemické receptory zaznamenávají změny kyselosti prostředí a koncentrace různých látek: cukrů, aminokyselin, kyslíku. Mnoho bakterií reaguje na změny teploty nebo světla a některé bakterie dokážou vnímat magnetické pole Země. Za nepříznivých podmínek se bakterie pokryje hustou skořápkou, cytoplazma je dehydratovaná a životně důležitá aktivita téměř ustane. V tomto stavu mohou bakteriální spory setrvat v hlubokém vakuu několik hodin a snášet teploty od –240 °C do +100 °C.